Microsoft word - 2900 002_stress_e_sonno.doc



Settembre – Novembre 2012
Stress e Sonno 2900.002
2900 Stress e Sonno
2900.1 Introduzione generale
2900.1.1 La neurologia perché
Oggigiorno, i problemi del SNC, relativi al comportamento individuale nella società moderna, sono diventati molto importanti per tutte le fasce di età. È ormai molto forte la loro incidenza nella vita quotidiana ed anche sul lavoro.
2900.1.2 Anatomia
2900.1.2.1 Introduzione
Il neurone è una cellula fondamentale del sistema nervoso, responsabile della conduzione degli stimoli.
2900.1.2.2
Struttura del neurone
Il neurone ha una forma irregolare: è dotato di una zona centrale, detta corpo cellulare o pirenoforo, e di un lungo prolungamento, l'assone; dal pirenoforo fuoriescono brevi prolungamenti ramificati, chiamati dendriti. In base al numero di prolungamenti che fuoriescono dal corpo cellulare, è possibile distinguere: neuroni multipolari, aventi numerosi dendriti e un singolo assone; i neuroni bipolari, dotati di un dendrite e un assone; i neuroni unipolari, caratterizzati da un unico prolungamento che fuoriesce dal corpo cellulare e si divide in un ramo centrale, con funzione di assone, e in uno periferico, con funzione di dendrite. I dendriti conducono gli impulsi in arrivo in direzione centripeta (cioè verso il corpo cellulare del neurone). I neuroni ricevono gli impulsi da altri neuroni: fanno eccezione quelli che si trovano nei recettori sensoriali che trasmettono, ad esempio, le informazioni di tipo termico o tattile dalla cute al cervello; in questo caso, il segnale viene generato da strutture specializzate poste nella cute, all'estremità del dendrite stesso. Gli assoni, o fibre nervose, conducono gli impulsi in direzione centrifuga (ovvero dal corpo cellulare verso l'esterno). Possono avere lunghezza molto variabile (nell'uomo, da 1 mm a 1 m). La membrana cellulare che riveste l'assone ha alcune caratteristiche che la differenziano da quella che avvolge la parte restante del neurone, e viene detta assolemma; il citoplasma contenuto al suo interno è indicato con assoplasma. Alle estremità degli assoni si trovano strutture a bulbo, chiamate bottoni sinaptici che formando le sinapsi e hanno il ruolo fondamentale di propagare l'impulso nervoso tra l'assone di un neurone e un dendrite di quello seguente, oppure da un assone a una ghiandola. Alcuni assoni prendono contatto con le fibre muscolari, formando strutture particolari, dette placche neuromuscolari. Diversi assoni, provenienti da neuroni differenti, si riuniscono in fasci per formare un nervo.
Stress e Sonno
2900.1.2.3
Sinapsi e trasmissione del flusso nervoso
Trasmissione dell'impulso nervoso nelle sinapsi A livello delle sinapsi, ossia delle strutture che collegano un neurone con il successivo, la trasmissione dell'impulso nervoso non avviene mediante lo spostamento di un'onda di depolarizzazione, come succede lungo la fibra nervosa (assone), ma attraverso la liberazione di molecole particolari, dette neurotrasmettitori. In risposta a una variazione del potenziale elettrico della membrana cellulare, a livello della terminazione dell'assone (o bottone sinaptico), si verifica la liberazione dei neurotrasmettitori che, diffondendo nello spazio della fessura sinaptica, si legano a specifici recettori posti sulla
membrana del neurone successivo. Tale legame produce alterazioni a livello della membrana della cellula nervosa, che inducono l'insorgenza di un potenziale elettrico e, quindi, permettono la propagazione dell'impulso. In base alla loro natura chimica, i neurotrasmettitori possono avere un'azione inibitoria o eccitatoria, cioè impedire o promuovere l'impulso stesso.
2900.1.3 La fitoterapia perché
I nostri antenati conoscevano bene le piante più correntemente usate per regolare l'umore, il sonno,
l'ansia e la depressione. All'occorrenza sono il Biancospino, il Papavero, il Luppolo, regolatori del
sonno, le labbiate aromatiche (Famiglia della Salvia e delle Ortiche) come la Lavanda e la Melissa,
l'Iperico, antidepressivo. La Valeriana (con qualche restrizione), la Ballotta e la Passiflora con le
loro proprietà antispasmodiche, antidepressive, antistress, sono un'alternativa efficace alle
benzodiazepine.
Studiamo adesso alcune affezioni neurologiche e comportamentali.
2900.2.1 Definizione
L'insonnia è l'assenza involontaria del riposo compensatore. Essa si manifesta con un'alterazione della qualità o della quantità del sonno con la conseguente ripercussione sull'attività diurna.
Stress e Sonno 2900.002
2900.2.2 Richiami di fisiologia
2900.2.2.1 Struttura del sonno
Il sonno ha una struttura molto precisa tanto da parlare di architettura del sonno. Si tratta di una successione di 4 o 5 cicli di 90 minuti ciascuno. Ogni ciclo si divide a sua volta in cinque stadi di diversa durata in funzione delle onde ritmiche emesse dal cervello. Gli stadi che vanno dal primo al quarto corrispondono al sonno lento mentre per il quinto si parla di sonno paradosso.
2900.2.2.1.1 Stadio
1
Si tratta della fase di assopimento con scomparsa progressiva delle onde alfa (onde della veglia) e apparizione delle onde theta.
2900.2.2.1.2 Stadio
2
Siamo nel sonno leggero. Il soggetto è completamente addormentato. Le onde alfa sono assenti e appaiono i segni caratteristici del sonno: i fusi accompagnati dai complessi K.
Stadi 3 e 4
Siamo nel sonno profondo, si nota la comparsa delle onde lente delta volte a sostituire progressivamente i fusi. Chi dorme è insensibile ai rumori e le sue funzioni vitali sono assicurate al minimo.
2900.2.2.1.4 Stadio
5
Quest'ultimo stadio che rappresenta circa il 20% del sonno totale è chiamato sonno paradosso perché all'elettroencefalogramma si nota la comparsa di onde simili a quelle della veglia.
Durante questo stadio appaiono dei rapidi movimenti oculari (REM: Rapid Eyes Movements); il tono muscolare si riduce al minimo; il ritmo cardiaco e respiratorio diviene irregolare e si sviluppa l'attività onirica.
Il dormiente alla fine dello stadio 5 ha terminato il suo ciclo anche se può di nuovo riapparire lo stadio
1 e cominciare così un nuovo ciclo. Questo nuovo stadio 1 che non dura più di qualche secondo, è
spesso impercettibile, salvo in caso di particolari circostanze: dolore, rumore, freddo, ecc.
Lo stadio 5 (sonno paradosso) chiude ogni ciclo di sonno.
Stress e Sonno
I differenti stadi del sonno hanno una durata variabile in funzione del ciclo durante il quale essi si svolgono. I primi due cicli comprendono tutti e cinque gli stadi del sonno con un sonno paradosso molto lungo (vedere schema). Si può costatare che c'è uno squilibrio fra il primo terzo della notte in cui si manifestano gli stadi del sonno profondo (stadio 3 e 4) e il resto della notte in cui predomina l'alternanza tra il sonno leggero (2) e il sonno paradosso (stadio 5). La durata del sonno paradosso per ciclo aumenta progressivamente nel corso della notte a discapito degli altri stadi.
Secondo i soggetti la durata totale di ogni stadio di sonno è variabile; tuttavia si può notare che la
quantità di sonno lento profondo (stadio 3 e 4) rimane relativamente costante anche se il bisogno di
sonno è differente da un individuo all'altro.
Ciò ci fa comprendere la sua importanza.
Il discorso cambia quando si parla di sonno paradosso. A tal proposito esistono grandi differenze;
infatti la sua durata aumenta notevolmente nei dormiglioni. Coloro che dormono più dei loro bisogni
aumentano la durata del sonno paradosso; sono più soggetti a sogni, incubi e spesso si svegliano
stanchi.
2900.2.2.2 Ruoli delle diverse strutture
Ogni stadio del sonno ha la sua importanza. Numerosi esperimenti condotti nei volontari hanno
permesso di valutare le funzioni dei rispettivi stadi. Alcuni soggetti, dopo essere stati privati del
sonno, modificano, al momento della loro prima notte di sonno, la ripartizione dei differenti stadi.
Si noterà un aumento del sonno profondo (3 e 4) che andrà a costituire il 70% della durata media dei
cicli.
L'organismo cerca di recuperare il sonno perduto favorendo gli stadi 3 e 4 che rappresentano il sonno
ristoratore dalla stanchezza. Il sonno paradosso, invece, permette al cervello di memorizzare gli
eventi antecedenti, i comportamenti, gli apprendimenti e ad eliminare la stanchezza fisica e nervosa.
Esperimenti condotti su soggetti svegliati sistematicamente ad ogni inizio del sonno paradosso,
hanno permesso di rilevare che l'assenza di sogni conduce progressivamente alla follia. Il sogno
è una necessità biologica.
Ogni stadio ha la sua importanza per cui al verificarsi di disturbi legati al sonno è indispensabile
utilizzare una terapia che rispetti nel miglior modo possibile l'architettura del sonno.
Stress e Sonno 2900.002
2900.2.2.3 Meccanismi del sonno
A livello della sostanza reticolare del tronco cerebrale, esistono un centro del sonno (nucleo del rafe)
e un centro del risveglio.
Il centro del sonno dipende da altre strutture cerebrali: il sistema talamo-corticale e il sistema
rinencefalo-ipotalarnico. Anche se ancora non ben definiti, esistono probabilmente degli altri fattori
d'induzione. Il sonno appare nel momento in cui accade una deconnessione della sostanza reticolare
con il resto del cervello. Tale fenomeno è favorito dalla stanchezza neuronale, dal confort della
posizione (posizione allungata o seduta) e dall'assenza d'informazioni sensoriali. L'insieme di queste
circostanze comporta una "disattivazione a catena".
L'avviamento biochimico del sonno risulterebbe prodotto dall'azione frenate dei nuclei noradrenergici
che intervengono sulla veglia. Si può osservare una diminuzione della noradrenalina cerebrale e
quindi un abbassamento dell'attività dei neuroni catecolaminergici. In un secondo tempo s'instaura
invece il sonno lento la cui comparsa è condizionata dalla stimolazione dei nuclei serotoninergici e
dalla liberazione di serotonina. Al momento del sonno paradosso c'è una riattivazione dei nuclei
noradrenergici con il tasso di serotonina che resta elevato. La noradrenalina interviene nella veglia e
nel sonno paradosso.
I nuclei noradrenergici e serotoninergici sono sotto il permanente controllo di differenti neuroni, in
particolare i neuroni colinergici e GABA-ergici.
Ritmi biologici
Numerosi fenomeni biologici avvengono in maniera ritmica in relazione all'alternanza veglia/sonno. Ogni variazione di qualità o quantità durante la notte può essere all'origine di eventuali disordini biologici.
2900.2.2.3.2 Endocrinologia
Un gran numero di secrezioni ormonali variano in maniera ciclica in rapporto al sonno e la maggior parte di esse corrispondono a quelle delle stimoline ipofisarie. Ad esempio, la secrezione del G. H. (Growth Hormone) aumenta rapidamente dal momento in cui si instaura il sonno lento per formare poi un picco nel primo terzo della notte. La secrezione di prolattina raggiunge il culmine alla fine della notte mentre in caso di privazione del sonno la variazione notturna di questi ormoni viene abolita. Sia il T.S.H. (tireostimolina) che l'L.H. rispettano una certa ritmicità raggiungendo il massimo nel cuore della notte. L'A.C.T.H. è invece indipendente dal sonno e la sua secrezione avviene secondo un ciclo costante in un periodo di 24 ore, sincronizzato con l'ambiente circostante. L'A.C.T,H. regola le secrezioni del cortisolo, che raggiungono la massima concentrazione al mattino e le variazioni nictemerali della temperatura il cui minimo si verifica alle 3 del mattino.
2900.2.2.3.3 Citologia
A livello cellulare esistono numerosi metabolismi che si sviluppano in maniera ciclica. In effetti, è durante la notte che le cellule epatiche ricostituiscono il loro stock di glicogeno. Riguardo alle cellule implicate nell'immunità, si assiste a un aumento del loro rinnovamento nella fase notturna. La risposta immunitaria e i suoi componenti seguono una certa ritmicità. La protezione dell'organismo si consolida durante la notte. I medicamenti possono quindi avere effetti d'intensità differente secondo l'ora di somministrazione. Queste differenti risposte dell'organismo sono oggetto di interessanti ricerche in particolar modo nel campo della "cronofarmacologia".
Stress e Sonno
Altre attività
Durante la notte si verificano numerosi altri processi fisiologici; un esempio è dato dall'aumento del tono vagale che provoca a livello polmonare una diminuzione del diametro bronchiale. Tutto ciò spiega la grande frequenza di crisi asmatiche notturne. Inoltre, è durante il sonno paradosso che accade l'aumento di secrezioni di renina.
Contrariamente a ciò che si pensa, la notte non è di tutto
riposo per il nostro organismo.
2900.2.3 I vari disturbi del sonno
Le manifestazioni dell'insonnia possono essere molteplici; ciò nonostante si tende a raggrupparle in
tre grandi categorie:
- difficoltà ad addormentarsi
- risvegli precoci
- frequenti risvegli notturni
2900.2.3.1 Difficoltà ad addormentarsi (insonnia iniziale)
In questo caso è lo stadio 1 ad allungarsi (in media non deve oltrepassare il 5% del sonno totale).
Questo tipo di insonnia è spesso dovuta ad uno stato di ipervigilanza o ad uno stato ansioso legato a
cause esogene.
2900.2.3.2 I risvegli precoci (insonnia terminale)
Questo tipo di insonnia è meno frequente di quella precedente e può essere il riflesso di disordini
fisiologici. I risvegli precoci sono spesso legati ad un'assunzione eccessiva di sonniferi.
2900.2.3.3 Frequenti risvegli notturni
Si tratta di una soppressione quasi completa del sonno dovuta ad un'ansietà acuta o ad uno stato
depressivo mascherato.
2900.2.4 Trattamento dell'insonnia
2900.2.4.1 Igiene di vita
Per evitare i disturbi del sonno si deve ricorrere in primo luogo a dei mezzi semplici, forse un po'
dimenticati, ma sicuramente molto utili…ad esempio rispettare una sana igiene di vita.
L'ora per coricarsi
È importante mettersi a letto quando si ha sonno ovvero quando la sera si fanno sentire i primi sintomi (sbadigli, diminuzione dell'attenzione, palpebre pesanti, intorpidimento, ecc.), senza desistere. Un ciclo di sonno sta per cominciare e se non si va immediatamente a letto, dopo mezz'ora sarà più difficile riuscire ad addormentarsi poiché l'organismo è di nuovo in piena forma. I disturbi nell'addormentarsi sono frequenti in caso di viaggi transmeridiani e di orari lavorativi irregolari o notturni.
Stress e Sonno 2900.002
È necessario pertanto un compromesso tra le esigenze di vita socio-professionali e quelle dei nostri bioritmi.
2900.2.4.1.2 Alimentazione
La cena deve essere leggera, completa ed equilibrata. Si consigliano piatti ricchi di glucidi e poveri di
alimenti grassi poiché questi, ristagnando per molto tempo nello stomaco, danno una sensazione di
pesantezza.
Gli zuccheri rapidi sono da evitare perché possono provocare un'ipoglicemia rebound nel cuore della
notte che può essere causa di risveglio.
2900.2.4.1.3 Bevande
Le bevande eccitanti (caffè, tè, bevande a base di caffeina) e l'alcool devono essere evitati la sera dai
sofferenti di insonnia.
2900.2.4.1.4 Attività
L'esercizio fisico ha degli effetti positivi sul sonno a condizione che sia praticato durante la giornata, evitando soprattutto gli sport pesanti nella tarda serata.
2900.2.4.1.5 Ambiente
Il soggetto deve avere a sua disposizione uno spazio gradevole, quindi un letto confortevole e una giusta temperatura ambientale, al riparo da stimolazioni luminose e sonore.
2900.3.1 Definizione
Lo stress è una reazione dell'organismo nei confronti di un'aggressione esterna.
Letteralmente stress significa sforzo, tensione, sollecitazione ed indica il logorio cui è sottoposto
ciascuno di noi per effetto degli accadimenti della vita. Anche gli animali e le piante sono sottomesse
a stress.
Lo stress è la conseguenza psichica e fisica di un'inadeguatezza tra le condizioni che subiamo e le
nostre risorse personali o ambientali per fronteggiarle.
Più precisamente, bisogna dire che la reazione di stress è una sindrome generale d'adattamento
generata da una forza esterna che induce una reazione sia del fisico che del mentale di un
organismo.
La reazione di stress è una reazione fisiologica dell'organismo che è nata nell'uomo della preistoria.
La reazione di stress è una preparazione dell'organismo ad un'azione.
Nel mondo moderno l'uomo è sottoposto ad una serie d'aggressioni alle quali non può rispondere con
un'azione fisica. In queste condizioni, tutta la preparazione all'atto fisico si produce, senza però
sboccare su l'atto proprio detto. Questo può condurre a incidenti acuti o a dei disturbi psicosomatici.
Esistono due tipi di fattori di stress: fattori fisici e fattori mentali.
2900.3.1.1 Fattori di stress fisici:
Gli esercizi fisici intensi
Le variazioni estreme di temperatura
La stazione eretta prolungata
Stress e Sonno
2900.3.1.2 Fattori di stress mentali:
Possono essere di origine:
Personali
Sociali
Famigliari
Professionali
Geografici
Finanziari
2900.3.2 Importanza della reazione allo stress
La reazione è collegata all'intensità, alla durata e al fattore di ripetizione dello stress. Interviene anche la capacità personale di adattarsi agli stress esterni.
2900.3.3 Meccanismo della reazione allo stress
Sono implicati il Sistema nervoso (SNC e SNA) e il sistema immunitario (SI). Siccome l'informazione è trasmessa tramite ormoni, il sistema endocrinologico (SE) è ugualmente coinvolto. Abbiamo una reazione totale di tutta la persona. La reazione coinvolge l'equilibrio profondo dell'individuo ovvero: la psiche, il corpo e lo spirito. In breve:
2900.3.3.1 Reazione di allarme
Si osserva da 6 a 48 ore dopo l'avvenire della situazione stressogena. Si traduce con un aumento
dell'attività simpatica. Si nota un aumento della secrezione di cortisolo. L'organismo si trova in fase
catabolitica. La temperatura diminuisce. La persona è pronta ad affrontare l'evento.
2900.3.3.2 Fase di resistenza
I valori tornano normali, l'adattamento alla situazione di stress è ottimo.
2900.3.3.3 Fase d'esaurimento
Se la situazione persiste o è eccessiva, la capacità di reazione dell'organismo è esaurita. Diciamo
che la capacita di adattamento è esaurita. Questa capacita reattiva è il fattore limitante della reazione
allo stress.
2900.3.4 Incidenza dello stress
Dal 50 al 60% delle assenze per malattia, ogni settore professionale incluso, sarebbero imputabili allo
stress da lavoro che induce certe patologie, grande stanchezza, emicranie, male di schiena,
esaurimento nervoso.
Stress e Sonno 2900.002
2900.3.5 Il costo sociale dello stress
In Svizzera verso la fine degli anni 90 il costo dello stress per gli svizzeri è stato stimato a 4,2 miliardi di CHF ovvero pari al 1,2% del PIL. Si sono contate le spese mediche, ivi comprese quelle dell'automedicazione, e le spese legate alle assenze o alla perdita di produzione.
2900.3.6 Stress e lavoro: rischi cardiovascolari
Secondo uno studio finlandese molto serio, lo stress al lavoro raddoppierebbe il rischio di decesso per malattia cardiaca! Studio condotto da Mika Kivimaki e la sua squadra del Finnish Institute of Occupational Health a Helsinki. Hanno seguito 812 impiegati, 545 uomini e 267 donne, durante 25 anni! Tutti lavoravano nella stessa impresa finlandese. A partire da esami clinici e di interrogatori, gli autori hanno misurato la tensione arteriosa, il tasso di colesterolo e l'indizio di massa corporale di questi impiegati. Questi ultimi hanno valutato anche il loro grado di stress grazie ad un questionario. Gli autori hanno scoperto così che le tensioni generate dal lavoro moltiplicano per due il rischio di decesso per malattia cardiaca. Hanno infine dimostrato che lo stress era un fattore aggravante dell'ipercolesterolemia. Fonte: British Medical Journal, 18 ottobre 2002
2900.3.7 Conseguenze dello stress, definizione del Karoshi
Le conseguenze dello stress al lavoro possono essere molteplici: dalla semplice ansietà alla morte per sfinimento, passando dalla depressione o dal suicidio.
2900.3.7.1 Karoshi
Il karoshi, è la morte per sfinimento.
In Giappone ogni anno, 10.000 persone muoiono così al lavoro. Uno studio del ministero della Salute
e del Lavoro giapponese ha mostrato che un uomo su quattro ha lavorato più di 80 ore supplementari
al mese di luglio 2002!
Un livello di carico che, secondo il ministero, espone chiaramente al karoshi.
2900.3.8 Principali piante anti stress
Tra le principali piante medicinali caratterizzate da tali proprietà, riveste un ruolo di primo piano il Ginkgo biloba; risultano utili anche in questo caso fitocomplessi ad attività adattogena, come la Rodiola, il Ginseng, l'Eleuterococco, la Schisandra, il The verde, così come altre sostanze naturali come la Pappa Reale e il Polline, che per la loro attività energetica e tonificante, per l'azione antiossidante, anti-radicali liberi, vitaminizzante e remineralizzante, sono indicati per quasi tutte le fasce di età. E' importante tuttavia associare a queste piante adattogene, che conferiscono maggiore vitalità, anche altre piante i cui principi attivi facilitino e migliorino il recupero delle energie, favorendo il rilassamento. Alcune piante sono particolarmente efficaci nel ridurre lo stato di tensione continua che si accompagna alla condizione di stress, come la Passiflora, lo Ziziphus spinosa, la Melissa, eccetera. Vediamo le principali caratteristiche di alcune di queste piante.
Stress e Sonno
2900.3.9 Rodiola una risposta efficace allo stress
Questa pianta aumenta la resistenza allo stress fisico e mentale, migliora la qualità del sonno e
regolarizza il tono dell'umore. Vedi anche 2900.6.7
È una pianta d'origine siberiana, definita come adattogena.
È usata da più di 3000 anni dai siberiani come elisir di lunga vita e per aumentare la resistenza alla
fatica e alle malattie e stimolare la forza. Studiata solo dai russi fino al crollo del muro, la rodiola è
conosciuta in Europa solo dall'inizio degli anni 90.
Il termine adattogena sta per indicare che la pianta è in grado di aiutare l'organismo a reagire in
condizioni avverse (fisiche, chimiche o altre condizioni stressanti).
L'uso di Rodiola è consigliato per accrescere la resistenza dell'organismo agli stress di varia natura e
in grado di migliorare il tono dell'umore e la lucidità mentale.
2900.3.10 Premesse scientifiche e storiche
La Rodiola è una pianta di recente introduzione nel bagaglio terapeutico occidentale.
Nel 1947 Lazarev introduce il termine di Adattogeno.
Nel 1969, Brekhman e Dardymov propongono un modello sperimentale per evidenziare le proprietà
adattogene. Il risultato mostra un aumento della secrezione delle beta endorfine. Questa
"ricompensa" fisiologica permette di superare e affrontare di nuovo lo stress.
Nell'ottobre 1975, dopo diverse ricerche cliniche in doppio cieco contro placebo, il ministero russo
della salute permise l'uso della Rhodiola rosea come pianta officinale.
2900.3.11 Pianta adattogena
Le piante di questo tipo (Rodiola, Ginseng, Eleuterococco) sono in grado di migliorare la resistenza dell'uomo a disordini legati agli stress ed aumentare in generale la capacità d'adattamento. Si tratta in pratica di un aiuto per l'organismo per diminuire la prima fase reattiva dello stress e di aumentare il ritorno alla normalità, evitando l'esaurimento della capacità reattiva dell'organismo. La Rodiola ad esempio sarebbe stata molto usata sia dagli atleti russi che dai cosmonauti per aumentare l'energia, capacità di resistenza e soprattutto aumentare la resistenza allo stress prolungato. Rhodiola rosea è un cardio-protettivo: normalizza la frequenza cardiaca dopo un esercizio fisico intenso, migliora le funzioni mentali come la memoria, aumentando la quantità di sangue nei muscoli e nel cervello. Sono anche dimostrate delle proprietà anabolizzanti muscolari. La Rodiola è anche un agente anti-deprimente.
Stress e Sonno 2900.002
2900.4 Depressioni
Depressione:
Disturbo dell'umore caratterizzato da sentimenti di malinconia, colpa, indegnità e disperazione.
I diversi tipi di depressioni:
Le depressioni
Depressioni primarie
Endogene Depressione malinconica
Psicosi maniaco-depressiva
Depressioni secondarie
A patologia somatica A patologia psichiatrica
2900.4.1 Depressioni primarie endogene
La depressione endogena è la forma tipica della malinconia.
Insorge senza ragioni.
Umore depressivo (perdita della voglia di fare).
Inibizione psico motrice.
Sintomi associati: ansia, risveglio presto, astenia.
Origine in relazione con fattori biologici?
2900.4.1.1 Psicosi maniaco depressiva (P.M.D.)
2900.4.1.1.1 Definizione
Questa patologia è alla frontiera tra la depressione e la psicosi.
Esistono due fasi:
2900.4.1.1.2 Accesso malinconico
Depressione a delirio con rischio suicidio importante.
Rallentamento psicomotorio estremo
2900.4.1.1.3 Accesso maniaco
Stato di sovra eccitazione fisica e psichica, vicina al delirio.
Umore euforico, attività psicomotoria intensa…
Stress e Sonno
2900.4.1.1.4 Evoluzione
2900.4.1.1.4.1 Bipolare:
Accesso maniaco + normotimia +accesso depressivo
2900.4.1.1.4.2 Unipolare depressivo (donna):
Accesso depressivo + normotimia + accesso depressivo
2900.4.1.1.4.3 Unipolare maniaco (raro):
Accesso maniaco + normotimia + accesso maniaco
2900.4.1.2 Depressione d'involuzione
Soggetti di età > 50 anni (donne in menopausa).
Inizio progressivo: Ipocondria + ansia.
< fattori esterni
2900.4.1.3 Depressione stagionale
Donne giovani (86%).
PMD bipolare con accessi malinconici in inverno
Sintomi: accessi bulimici con aumento di peso, con ripiego su se stessi, ipersonnia.
Causa: mancanza di luce? (Fototerapia).
2900.4.1.4 Depressione mascherata
Sintomi depressivi mascherati da
2900.4.1.4.1.1 Disturbi somatici:
Dolori, astenia, insonnia, disturbi digestivi.
2900.4.1.4.1.2 Comportamenti patologici:
Anoressia, alcolismo…
2900.4.1.4.2 Indici
2900.4.1.5 Depressione psicogena
Umore triste però moderato e fluttuante, recettivo alle sollecitazioni dei famigliari
Rallentamento
Sintomi: ansia, disturbi del sonno, disturbi dell'alimentazione, disturbi sessuali
2900.4.1.6 Depressione nevrotica
Il paziente riattiva una frustrazione dell'infanzia, all'occasione di un evento particolare. Rivive una
sensazione d'abbandono.
2900.4.1.7 Depressione per spossatezza
Breve nel tempo
Legata ad una spossatezza affettiva su un paziente sottomesso a stress continuo e durevole
(eccesso di lavoro…)
Stress e Sonno 2900.002
2900.4.1.8 Depressione di reazione
Legato ad un evento traumatico unico: lutto, incidente di un figlio, divorzio…
2900.4.1.9 Disturbi distimici
Episodio depressivo che dura dai 2 mesi ai 2 anni al massimo.
Doppia depressione: episodio depressivo in terreno distimico
Trattamento:
2900.4.1.10
Depressione breve e ricorrente
Di recente introduzione
Gli episodi depressivi durano solo qualche giorno.
2900.4.2 Trattamento medicamentoso classico
2900.4.2.1 Farmaci antidepressivi triciclici
Un gruppo di farmaci di largo impiego è quello dei cosiddetti antidepressivi triciclici, come
L'amitriptilina
ROCHE SIT
La clomipramina
NOVARTIS
ANAFRANIL 10
ANAFRANIL 25
La desipramina.
L'imipramina
TOFRANIL 10TOFRANIL 25
Alcuni sono particolarmente utili per i casi di pazienti insonni, altri, per contro, si adattano a soggetti che lamentano una continua sensazione di torpore; possono però causare effetti collaterali come aritmie del battito cardiaco, stipsi, annebbiamento della vista, vertigini. Costituiscono spesso il primo tipo di farmaci che il medico prescrive.
2900.4.2.2 Antidepressivi IMAO
2900.4.2.3 I.M.A.O. = Inibitori delle monoamminossidasi Un altro gruppo di farmaci è quello degli IMAO, o inibitori delle monoamminossidasi. Le monoamminossidasi sono enzimi normalmente deputati alla distruzione delle molecole di neurotrasmettitore, quando queste hanno svolto la loro funzione nella conduzione degli impulsi nervosi; poiché nel paziente depresso i neurotrasmettitori serotonina o noradrenalina sono prodotti in
Stress e Sonno
quantità insufficiente, un farmaco che blocchi l'azione di questi enzimi può permettere un aumento della quantità dei neurotrasmettitori stessi; tale azione è infatti svolta dagli IMAO. Questi composti sono ora di scarso impiego, poiché la loro assunzione comporta una particolare dieta, in cui sono eliminati o limitati i cibi contenenti una sostanza detta tiramina (come molti formaggi, pesce affumicato, bevande alcoliche); possono inoltre esercitare dannose interazioni con altri composti farmaceutici e provocare uno stato di ipertensione. Alcuni IMAO di recente introduzione:
toloxatone
moclobemide
sembrano ancora comportare rischi.
2900.4.2.4 Antidepressivi inibitori del reuptake della serotonina
Il fenomeno del reuptake della serotonina consiste nel riassorbimento di questo neurotrasmettitore a
livello delle sinapsi nervose, attraverso la membrana della terminazione presinaptica.
Poiché la serotonina nei pazienti depressi è sintetizzata a livelli insufficienti, i farmaci che ne
inibiscono il riassorbimento ne determinano indirettamente un aumento di concentrazione, e possono
alleviare alcuni disturbi connessi alla depressione.
Questo gruppo di farmaci, tra cui sono compresi:
la fluoxetina cloridrato
la paroxetina
è più recente di quello dei triciclici, e sembra produrre minori effetti a livelli dell'apparato circolatorio. Questi antidepressivi possono però produrre nausea, diarrea e cefalea.
2900.4.3 Effetti collaterali dei farmaci antidepressivi
di Fornaro P., Baconcini C., Fiscella G., Miccoli E.
Dipartimento di Scienze Psichiatriche dell'Universita' di Genova (Direttore Prof. R. Rossi)
RIASSUNTO: I farmaci antidepressivi, estremamente eterogenei per struttura chimica e meccanismo
d'azione, sono indicati nel trattamento di un vasto ambito di condizioni psichiche. Queste sostanze
possono determinare effetti collaterali, o secondari, che solitamente precedono l'effetto terapeutico o
principale. Vengono descritte manifestazioni collaterali principalmente a carico di: apparato digerente,
apparato cadiocircolatorio, apparato genitourinario e sistema nervoso.
Oltre ad una corretta scelta del tipo di farmaco, delle dosi e della modalità di somministrazione, è di
fondamentale importanza che il medico fornisca al paziente, ed eventualmente ai suoi familiari,
informazioni chiare e complete sui possibili effetti collaterali, al fine di instaurare una valida relazione
medico-paziente ed evitare precoci interruzioni della terapia prescritta.
Il trattamento terapeutico dei pazienti affetti da Disturbi dell'Umore e/o Disturbi d'Ansia si fonda
comunemente sull'impiego di farmaci antidepressivi .
Queste sostanze consistono in una lunga serie di derivati tra loro eterogenei quanto a struttura
chimico molecolare, destino metabolico cui vanno incontro nell'organismo e tipo di effetti biochimici e
clinici indotti dalla loro somministrazione.
Le manifestazioni cliniche degli antidepressivi, come del resto quelle di qualsiasi altro farmaco
(compreso lo stesso placebo), comprendono sia l'effetto terapeutico o principale, che rappresenta
l'obiettivo del trattamento, sia effetti collaterali o secondari che in genere precedono l'insorgenza della
Stress e Sonno 2900.002
risposta terapeutica e si attenuano fino a scomparire per il rapido intervento di meccanismi di adattamento recettoriale. A seconda dei casi, gli effetti collaterali degli antidepressivi potranno risultare insignificanti e quindi trascurabili dal punto di vista clinico, oppure utili per un più tempestivo controllo di determinate manifestazioni del disturbo (ad esempio gli effetti sedativo ed ipnoinducente indotti dal farmaco nel paziente depresso, ansioso ed insonne) oppure, infine, indesiderati perché dannosi o semplicemente fastidiosi e comunque tali da compromettere la regolare assunzione del farmaco ("compliance") e quindi il successo della terapia . La natura, la gravità e la durata degli effetti collaterali degli antidepressivi dipendono da molteplici fattori relativi al paziente, al farmaco, al medico, al tipo di rapporto medico-paziente ed all'ambiente in cui il trattamento farmacoterapeutico viene posto in atto. Ovviamente al medico sono richieste l'abilità e la competenza necessarie perché l'impiego di un determinato antidepressivo risulti sicuro ("primum non nocere") e, quindi, clinicamente efficace. Il raggiungimento di tale obiettivo passa attraverso la personalizzazione della scelta del tipo di farmaco, delle dosi, delle modalità di somministrazione e, al tempo stesso, attraverso una corretta impostazione e conduzione del rapporto medico-paziente. Il necessario rapporto di fiducia e collaborazione tra il paziente ed il terapeuta si sviluppa e si consolida se vengono preliminarmente fornite chiare e complete informazioni circa il tipo, l'entità', il significato ed il carattere transitorio degli effetti collaterali che possono emergere durante la fase iniziale del trattamento e persistere fino alla comparsa della risposta terapeutica.
FARMACI ANTIDEPRESSIVI
A partire dal 1958, anno della scoperta casuale degli effetti sul tono dell'umore dell'Imipramina e dell'Iproniazide, farmaci capostipiti rispettivamente della classe degli antidepressivi triciclici e di quella degli inibitori delle monoaminoossidasi (IMAO), sono stati adottati nella prassi psichiatrica numerose altre sostanze che si sono rivelate efficaci per il trattamento dei disturbi depressivi e d'ansia (disturbi fobici, disturbi da attacchi di panico, disturbo ossessivo compulsivo, disturbi della condotta alimentare, ecc). L'eterogeneità delle sostanze oggi disponibili è tale per cui risulta problematica una loro soddisfacente classificazione:
A) Inibitori del reuptake delle monoamine
I) Non selettivi a)Triciclici : amine terziarie (Imipramina, Clorimipramina, Amitriptilina, Trimipramina): amine secondarie (Nortriptilina, Desipramina) b) Non Triciclici: Inibitori del "Reuptake" della Serotonina e della Noradrenalina SNRI (Venlafaxina) II) Selettivi (Fluoxetina, Fluvoxamina, Paroxetina, Sertralina, Citalopram,ecc.)
B) Farmaci che con meccanismo differente potenziano la trasmissione
- Noradrenergica (Maprotilina, Mianserina, ecc.) - Serotoninergica (Trazodone, Nefazodone, ecc.) - Dopaminergica (Amineptina, Minaprina, ecc.)
C) Altri farmaci
S-adenosil metionina, Folati, Sali di Litio, Rubidio, 5-Idrossi Triptofano
D) Inibitori delle monoaminoossidasi IMAO o Anti MAO
Stress e Sonno
I) Classici, non selettivi e ad azione irreversibile (Fenelzina, Tranilcipromina, Iproniazide, ecc.)
II) Selettivi e Reversibili
a) IMAO di tipo B (Deprenile o Selegilina)
b) IMAO di tipo A (Moclobemide, Brofaromina, Toloxatone)
Gli effetti collaterali (e terapeutici) degli antidepressivi, sono entro certi limiti correlati con gli effetti
provocati dal farmaco a livello neurotrasmettitoriale e recettoriale:
Effetti neurotrasmettitoriali e recettoriali degli antidepressivi:
- Blocco dei recettori per:
l'acetilcolina, l'istamina, la noradrenalina la serotonina
- Inibizione del "reuptake" della noradrenalina e/o dopamina
- Attivazione della liberazione ("release") della noradrenalina o dopamina o serotonina
- Riduzione della sensibilita' e del numero di determinati recettori (alfa1, alfa2 e beta per la
noradrenalina, recettori D2 per la dopamina, sottotipi recettoriali per la serotonina, ecc.)
- Inibizione delle monoaminoossidasi "A e B","A","B"
Questi effetti variano a seconda delle fasi del trattamento e a seconda de tipo di farmaco: ogni
derivato pertanto presenta un suo particolare profilo farmaco dinamico dal quale in larga misura
dipende il suo profilo clinico, vale a dire il tipo di manifestazioni terapeutiche e collaterali provocate
dalla sua somministrazione.
Gli effetti degli antidepressivi riguardano differenti organi sistemi ed apparati:
- Effetti a carico dell'apparato digerente.
Soprattutto i derivati più capaci di effetti anticolinergici (triciclici a struttura aminica terziaria e, meno facilmente, triciclici a struttura aminica secondaria ed IMAO non reversibili e non selettivi), possono provocare secchezza della bocca e delle fauci (con rischio di stomatiti e carie dentaria) per cui sono utili l'assunzione di liquidi, l'impiego di chewing gum senza zucchero e/o di preparati di saliva artificiale. In rari casi possono verificarsi inoltre difficoltà di deglutizione e/o esofagiti. A livello gastrico possono essere lamentati senso di sazietà, difficoltà digestiva, bruciori, nausea e talora vomito (più frequenti con i farmaci più potenti nell'attivare la trasmissione mediata da Serotonina, farmaci responsabili spesso anche di diarrea); a livello intestinale, invece, stitichezza (che può risultare problematica nei soggetti affetti da emorroidi, ragadi ecc. e nei pazienti anziani o comunque predisposti per rischio di ileo paralitico). In tali casi occorre che il paziente assuma maggiori quantità di liquidi, di sostanze alimentari ricche di fibre e lassativi. Questi effetti, legati all'attività anticolinergica degli antidepressivi, possono essere attenuati dalla somministrazione di Betanecolo. A livello epatico gli antidepressivi, in genere, possono provocare un transitorio ed irrilevante aumento delle transaminasi; gli IMAO ad azione irreversibile e non selettiva possono essere responsabili di epatotossicità ( talora con ittero epatocellulare).
- Effetti a carico del sistema cardiocircolatorio.
Gli antidepressivi triciclici (soprattutto quelli a struttura aminica terziaria) e gli IMAO ad azione irreversibile e non selettiva, possono facilmente indurre ipotensione arteriosa, ipotensione ortostatica (con rischio di cadute e traumi particolarmente negli anziani) e crisi di tachicardia. I farmaci SSRI, invece, possono provocare bradicardia, mentre quelli SNRI, come la Venlafaxina, possono indurre un pur modesto aumento della pressione arteriosa. Gravi e rischiose crisi ipertensive (talora fatali) possono essere provocate dagli IMAO ad azione irreversibile e non selettiva nel caso in cui questi farmaci vengano erroneamente utilizzati. Il loro impiego presuppone infatti che il paziente non assuma bevande (vino, birra, alcolici, te', caffè,)
Stress e Sonno 2900.002
alimenti (yogurt formaggi fermentati, cacciagione, cibi non ben conservati, interiora di pollo, cibi preparati con lievito di birra, legumi) o medicamenti (anestetici, vasocostrittori, analgesici, altri antidepressivi ecc.) che potranno essere nuovamente assunti dopo un periodo di almeno 15 giorni dalla sospensione del trattamento con IMAO. Questi ultimi inoltre possono essere prescritti solo dopo 7-10 giorni dalla interruzione di antidepressivi triciclici e non prima che siano trascorsi 30 giorni dall'assunzione dell'ultima dose di Fluoxetina. Questo farmaco, infatti, al pari degli altri SSRI, interagisce pericolosamente con gli IMAO determinando una sindrome serotoninergica con alterazioni psichiche quali eccitamento ipomaniacale, irrequietezza, mioclono, iperreflessia, ipersudorazione, brividi, diarrea, febbre, tremori e disturbi della coordinazione motoria (Strenbach H; 1991). Gli antidepressivi triciclici (soprattutto le amine terziarie) possono provocare alterazioni del tracciato elettrocardiografico (ECG) con un aumento della durata degli intervalli PR, QRS e QT. Questi farmaci, quindi, vanno impiegati con cautela nei soggetti che presentano disturbi della conduzione del miocardio. Più in particolare, nei soggetti depressi cardiopatici con disturbi di conduzione di lieve entità, quali il blocco atrioventricolare (BA-V) di secondo grado tipo Mobitz 1, blocco di branca destro, emiblocco anteriore sinistro, gli antidepressivi triciclici vanno impiegati con grande prudenza e con regolari controlli ECG. In caso di BA-V più grave, quale il BA-V di secondo grado tipo Mobitz 2, l'impiego dei triciclici è assolutamente controindicato. Nei soggetti cardiopatici risultano più sicuri gli anti-MAO e gli SSRI (Glassman, 1993).
- Effetti a carico dell'apparato genitourinario.
Gli antidepressivi triciclici possono provocare difficoltà nella minzione, ritenzione urinaria ed un aggravamento di un'eventuale ipertrofia prostatica (nei pazienti affetti da questo disturbo gli antidepressivi triciclici, come tutti i farmaci con azione anticolinergica, sono assolutamente controindicati). Altri effetti collaterali consistono in disturbi sessuali quali riduzione della libido, disturbi dell'erezione, anorgasmia, alterazioni dell'eiaculazione (che può essere talora ritardata od assente, talora dolorosa o retrograda), priapismo (in soggetti in trattamento con Trazodone). Ulteriori manifestazioni consistono in iperprolattinemia, disturbi del ciclo mestruale fino all'amenorrea, galattorrea, ginecomastia: Questi ed altri effetti endocrini e metabolici (soprattutto a carico del metabolismo degli zuccheri, nonché l'effetto di "craving" per i carboidrati), sono responsabili dell'aumento di peso corporeo indotto dalla maggior parte dei farmaci antidepressivi.
- Effetti collaterali a carico del sistema nervoso.
Altri importanti effetti collaterali riguardano il sistema nervoso e comprendono manifestazioni neurologiche e psichiche.
- Effetti collaterali neurologici.
Gli antidepressivi (soprattutto gli IMAO) possono, sia pur raramente, provocare disturbi della sensibilità (parestesie) conseguenti a neuropatie che verosimilmente dipendono da carenza di piridossalfosfato. Altri effetti collaterali sono tremore a scosse fini, acatisia (impossibilità a mantenere oltre un breve lasso di tempo una determinata posizione per un incoercibile bisogno di muoversi) ed in altri sintomi extra piramidali che richiamano il Morbo di Parkinson. Queste manifestazioni, più comunemente indotte dai farmaci neurolettici, possono talora verificarsi anche a seguito di somministrazione di antidepressivi e, in particolare, dei derivati SSRI. Altri effetti neurologici degli antidepressivi consistono nelle mioclonie e nelle crisi epilettiche che si possono verificare in soggetti predisposti per l'abbassamento della soglia convulsivante provocato da tali farmaci. Il rischio di crisi e' massimo nel caso della Maprotilina, minimo in quello della Viloxazina e dei derivati SSRI Infine, gli antidepressivi provocano facilmente astenia e, talora, sedazione eccessiva, rallentamento psicomotorio, disturbi della coordinazione motoria e cefalea.
- Effetti collaterali psichici.
Stress e Sonno
Astenia, sedazione, rallentamento psicomotorio, sonnolenza o, viceversa, ansia, irrequietezza psicomotoria, irritabilità, insonnia e peggioramento dei sintomi deliranti ed allucinatori in pazienti psicotici, sono manifestazioni collaterali che possono facilmente verificarsi durante la fase iniziale del trattamento con antidepressivi. Con riferimento a tali effetti, in passato si è tentato di caratterizzare i vari farmaci antidepressivi in derivati ad azione prevalentemente sedativa (Amitriptilina, Trimipramina, Doxepina, ecc.) o disinibente (IMAO, Nortriptilina, Desipramina ecc.). Gli antidepressivi, soprattutto i derivati triciclici a struttura aminica terziaria, meno facilmente quelli delle altre classi, possono provocare disturbi dell'attenzione, della concentrazione e della memoria fino a determinare stati confusionali ("delirium") con disorientamento temporo-spaziale, agitazione psicomotoria, allucinazioni, deliri ecc., effetto di più facile riscontro in soggetti predisposti da alterazioni cerebrali organiche. I derivati SSRI, in genere, non provocano né sedazione né alterazioni cognitive: per tale motivo, oltre che per la loro irrilevante azione anticolinergica, alfa1 noradrenolitica ed antistaminica, questi farmaci sono da considerare di prima scelta negli anziani e nei pazienti affetti da patologie concomitanti che controindichino l'impiego di antidepressivi triciclici. Un impiego prudente e limitato nel tempo degli antidepressivi si impone nel caso in cui i pazienti depressi soffrano di disturbi bipolari dell'umore: questi farmaci possono infatti favorire il viraggio della sintomatologia depressiva in senso ipomaniacale o francamente maniacale o, ancora, indurre o peggiorare un decorso a cicli rapidi della patologia.
Altri effetti collaterali.
Sia pur raramente, gli antidepressivi triciclici possono indurre effetti collaterali ematologici (diminuzione del numero dei globuli bianchi e delle piastrine, aumento degli eosinofili e dei linfociti ipo o iperglicemia, iponatriemia, ecc), dermatologici (ipersudorazione, rash, porpora, petecchie, prurito, orticaria, dermatiti, edema facciale, fotosensibilizzazione cutanea ecc.). Piu' frequenti invece sono gli effetti collaterali a carico dell'occhio e la funzione visiva quali midriasi con possibile presbiopia, cicloplegia con talora visione offuscata, riduzione della lacrimazione, e insorgenza, in soggetti predisposti, di glaucoma ad angolo acuto, patologia che rappresenta una controindicazione assoluta all'impiego di antidepressivi con attività anticolinergica.
CONCLUSIONE
I farmaci antidepressivi sono indicati nel trattamento delle varie fasi (iniziale, di mantenimento e
preventiva) di un vasto ambito di condizioni psichiche che comprendono, oltre alle varie forme della
depressione, disturbi di ansia quali in disturbo di attacchi di panico, i disturbi fobici, il disturbo
ossessivo compulsivo, i disturbi della condotta alimentare ecc.
Durante le prime settimane di trattamento, tali farmaci possono indurre effetti collaterali che, in
genere, precedono l'insorgenza dell'effetto terapeutico.
Una corretta scelta del tipo, delle dosi e delle modalità di
somministrazione, scelta che deve essere effettuata con
riferimento costante al criterio del massimo grado di sicurezza e al
tempo stesso di efficacia, e il presupposto indispensabile per
minimizzare il rischio che insorgano effetti collaterali indesiderati.
Questi ultimi sono il risultato non solo delle caratteristiche del farmaco, variabili da derivato a derivato
per cui ogni antidepressivi ha una propria identità chimico-farmacologica ed un suo potenziale di
provocare determinati effetti clinici, ma anche delle varie caratteristiche (cliniche psicologiche,
situazionali) del paziente, le quali condizionano il vissuto del farmaco e la risposta psicologica ad i
suoi effetti.
Stress e Sonno 2900.002
Un corretto approccio al paziente e lo strutturarsi di un valido rapporto di fiducia e di collaborazione tra medico, paziente e familiari, prevedono anche l'informazione chiara e completa circa la possibilità che prima ancora che si determini la risposta terapeutica, compaiano effetti collaterali indesiderati. Sarà così possibile evitare la compromissione della relazione medico-paziente e la prematura interruzione dell'assunzione della terapia prima che questa abbia avuto successo.
2900.5 Consigliare le piante della linea blu
Prima di dare un qualsiasi consiglio al proprio paziente occorre sempre ricordare delle semplici
indicazioni d'igiene di vita.
Per i problemi di sonno
Ricordare di non bere bevande eccitanti o alcoliche prima di andare a letto.
Andare al letto ai primi segni del sonno.
Non rimanere mai a guardare la TV, ad esempio se si ha sonno.
In regola generale, è sempre meglio andare a letto presto e alzarsi presto che l'inverso.
Problemi di ansia
Cercare di pensare a qualcos'altro prima di andare a letto.
Non leggere mai a letto prima di dormire.
Non aspettare di prendere rimedi al momento di coricarsi, ma almeno ½ ora prima.
Problemi di depressione
Isolarsi non fa bene.
Sforzarsi di stare in compagnia.
Stare alla luce il più possibile, non dormire al buio totale.
Esempio:
Quando vado a letto, mi tornano in mente tutti i miei problemi e non riesco a prendere
sonno…
Diminuire l'ansia
Favorire il sonno: VALERIANA Consiglio: per 4 settimane
2 caps di Passiflora prima di cena,
2 di Valeriana ½ ora prima di andare a letto
Ho degli attacchi di panico soprattutto la sera o quando vado a letto
Diminuire l'agitazione:
Aumentare la tranquillità
Consiglio: per 2 cicli di 3 settimane interrotti da un "riposo di 10 giorni"
2 caps di Biancospino a colazione
2 di Melissa prima di pranzo
2 di Melissa prima di cena
2 caps di Biancospino prima di coricarsi
Sono agitata, il mio lavoro mi stressa non riposo bene
Stress e Sonno
Diminuire gli effetti dello stress:
Favorire il sonno: VALERIANA Diminuire la reattività:
Consiglio: per 8 settimane
2 caps di Rodiola alla mattina a colazione
2 caps di Biancospino a pranzo
2 caps di Rodiola prima di cena
2 caps di Valeriana prima di coricarsi
Stress e Sonno 2900.002
Di notte mi risveglio e devo mangiare qualche cosa
Rilassarsi e diminuire la fame nervosa:
Ridurre i risvegli notturni:
Consiglio: per almeno 1 mese, magari 2
2 caps di Melissa in fine pomeriggio
2 di Melissa e di Escolzia ½ ora prima di coricarsi
Mi rigiro nel letto prima di addormentarmi
Diminuire l'agitazione:
Tranquillizzarsi:
Consiglio: per cicli di 3 settimane interrotte da 1 settimana senza niente
2 caps di Luppolo a cena
2 di Passiflora ½ ora prima di coricarsi
Mi sento depresso, dormo poco
Depressione:
Consiglio: per almeno8 settimane
2 caps di Rodiola a colazione
2 di Rodiola a cena
1 di Iperico ½ ora prima di andare a letto
Stress e Sonno

2900.6 Fitoterapia, Linea Blu
Stress e Sonno 2900.002

2900.6.1 BIANCOSPINO, Crataegus laevigata, Rosaceae
Il Biancospino è una delle piante medicinali più antiche
usate nella medicina europea: veniva usata anche
nell'antica Grecia dove per la prima volta è stata scoperta
l'azione curativa del Biancospino sul cuore. Il Biancospino
ha proprietà ansiolitiche e antispasmodiche ed è
tradizionalmente utilizzato nel trattamento di stati di ansia e
di disturbi del sonno negli adulti. Il Biancospino è un tonico
cardiaco che rinforza, protegge e dà tono al sistema
cardiovascolare. RR
2900.6.1.1 Luogo di origine
Europa
2900.6.1.2 Droga
Sommità fiorita.
Si dosano i flavonoidi (minimo 1,5% di flavonoidi totali
espressi in Iperosidi).
2900.6.1.3 Principi attivi
Flavonoidi (2%) di tipo Flavoni e Flavani ad azione inotropa positiva e cronotropa negativa.
Kaempferolo, quercitina, iperoside e vitexina; proantocianidine oogomeriche (3%).
Amine piogene: feniletilamina, O-metossifeniletilamina e tiramina, tannini, glicosidi cianogenetici e
saponine
2900.6.1.4 Punto d'impatto
Cuore, vasi arteriosi SNA e SNC
2900.6.1.5 Proprietà
Inotropo positivo (aumento della forza di contrazione del cuore) riconducibile all'inibizione della
AMP-c fosfodiesterasi da parte dei flavonoidi,
Cronotropo negativo (riduzione della frequenza cardiaca),
Dromotropo positivo (aumento della conduzione atrio-ventricolare)
Batmotropo negativo (riduzione dell'eccitabilità cardiaca).
Ipotensiva, sedativa, antispasmodica, cardiotonica, vasodilatatrice coronarica
2900.6.1.6 Presentazione
350 mg di polvere criofrantumata di sommità fiorita di Biancospino per capsula.
Stress e Sonno
2900.6.1.7 Indicazioni
Angina pectoris
Insonnia negli adulti e nei bambini
Ipertensione arteriosa
Disturbi del sonno
Pratica dello Sport
Eretismo cardiaco
Stanchezza fisica
Insonnia d'origine nervosa
Turbe della menopausa
2900.6.1.8 Posologia
1 o 2 Arkocapsule 2 volte al giorno
2900.6.1.9 Fitovigilanza1
Il Biancospino (Crataegus oxyacantha, Crataegus monogyna) è comunemente utilizzato come
cardiotonico di mantenimento nel trattamento dello scompenso cardiaco, come antiaritmico ed
antiipertensivo. È inoltre utilizzato per il trattamento dell'insonnia, di stati ansiosi e di disturbi
gastrointestinali.
I principali componenti della pianta, presenti nelle foglie e nelle sommità fiorite, comprendono:
flavonoidi (quali kaempferolo, quercitina, iperoside e vitexina; proantocianidine), amine biogene (quali
feniletilamina, O-metossifeniletilamina e tiramina), tannini, glicosidi cianogenetici e saponine.
A livello cardiaco il biancospino determina un effetto inotropo positivo (aumento della forza di
contrazione del cuore) riconducibile all'inibizione della AMP-c fosfodiesterasi da parte dei flavonoidi,
un effetto cronotropo negativo (riduzione della frequenza cardiaca), un effetto dromotropo
positivo (aumento della conduzione atrio-ventricolare) ed un effetto batmotropo negativo (riduzione
dell'eccitabilità cardiaca).
La pianta determina inoltre rilascio della muscolatura liscia vasale con conseguente vasodilatazione
(in particolare a livello coronarico) e riduzione delle resistenze periferiche.
L'effetto sedativo è stato invece attribuito alle proantocianidine.
In vitro numerosi costituenti del biancospino hanno mostrato la capacità di inibire la biosintesi di
trombossano A2. Pertanto la somministrazione concomitante di farmaci antiaggreganti piastrinici e di
prodotti erboristici contenenti biancospino può comportare un maggiore rischio di sanguinamento.
Tale associazione dovrebbe quindi essere evitata.
Inoltre i prodotti a base di biancospino possono potenziare l'effetto della digossina attraverso un
meccanismo di tipo farmaco dinamico. In un recente studio condotto su 8 volontari sani, sottoposti
per tre settimane alla somministrazione concomitante di digossina (0.25 mg al giorno) e Biancospino
(450 mg due volte al giorno), è stato osservato che alle dosi utilizzate i parametri farmacocinetici della
digossina non vengono alterati dalla contemporanea somministrazione di biancospino. Pertanto, in
queste condizioni terapeutiche gli autori ritengono tale associazione piuttosto sicura. Infine, possibili
interazioni farmacologiche possono manifestarsi associando il biancospino a farmaci antipertensivi,
antianginosi ed antiaritmici.
2900.6.1.10 Bibliografia
Vedi: 2900.6.9.1
1 A cura di Alessandro Oteri, Dipartimento Clinico e Sperimentale di Medicina e Farmacologia, Università degli Studi di Messina
Stress e Sonno 2900.002
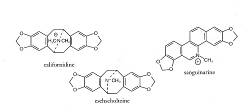
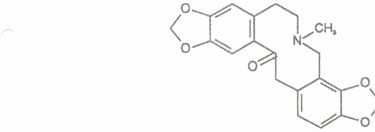

2900.6.2 ESCOLZIA, Eschcholzia californica, Papaveraceae
2900.6.2.1 Droga
Parte aerea fiorita. RR.
2900.6.2.2 Composizione chimica
Protopina ad azione anticolinergica e anti spastica.
2900.6.2.3 Principi attivi ad azione sedativa
Alcaloidi a nuclei isochinoleici, ad azione sedativa.
Titolazione dallo 0,8% all' 1,2% in alcaloidi totali espressi in Californidina.
2900.6.2.4 Punto d'impatto
SNC, Muscoli
2900.6.2.5 Proprietà
Sedativa, Ipnotica, Spasmolitica, Analgesica,
Stress e Sonno
2900.6.2.6 Indicazioni
Affaticamento intellettivo
Esaurimento nervoso
Colica intestinale
Colon irritabile
Insonnia da stress
Difficoltà a prendere sonno nell'adulto e nel
Risvegli notturni
Distonia neurovegetativa
Disturbi del sonno
Stanchezza intellettiva
2900.6.2.7 Posologia
1 o 2 Arkocapsule 2 volte al giorno
2900.6.2.8 Bibliografia
Vedi: 2900.6.9.2
Stress e Sonno 2900.002
2900.6.3 IPERICO, Hypericum perforatum, Hypericaceae
Per essere presentato come integratore alimentare,
l'apporto giornaliero in ipericina non deve essere superiore a 0,7 mg. al giorno.
Rapporto iperforine/ipericina non superiore a 7, comprendendo nella voce "iperforine" la
somma dell'iperforina e dell'adiperforina presenti nell'estratto.
L'Hypericum è utilizzato in Omeopatia contro i dolori d'origine nervosa.
2900.6.3.1 Origine
Europa e Asia occidentale, cresce spontaneamente lungo le strade.
2900.6.3.2 Droga
Foglie e sommità fiorite. RR
Deve contenere 0,08 % d'Ipericine espresse in Ipericina.
Stress e Sonno
2900.6.3.3 Punto d'impatto
SNC, SNA, Cute, Mucose
2900.6.3.4 Proprietà
Antidepressiva, sedativa, protettiva cute e mucose
2900.6.3.5 Indicazioni
Balbuzie
depressione leggera
Depressione mascherata
Depressione reattiva
Distonia neurovegetativa
Tic
Disturbi dell'umore
Ulcera gastroduodenale
Enuresi notturna
2900.6.3.6 Posologia
1 Arkocapsule 1 volta al giorno
2900.6.3.7 Fitovigilanza2
Erba di San Giovanni (Iperico). Interazioni con farmaci.
È una pianta ampiamente diffusa, nota nei paesi anglosassoni come erba di S. Giovanni (St. John Wort). I fiori sono la parte della pianta da cui si ottengono gli estratti normalmente utilizzati.
Da sempre utilizzato per diverse patologie, recentemente l'iperico ha raggiunto grande popolarità per
la sua efficacia nell'alleviare la depressione di grado lieve moderato (1, 2). Fra le sostanze dell'iperico,
implicate in questa azione, vi sarebbero l'ipericina, l'iperforina e i flavonoidi (3, 4, 5), il cui meccanismo
d'azione sarebbe da riportare ad una attività sui neurotrasmettitori cerebrali, quali serotonina,
dopamina e noradrenalina (3).La dose media normalmente utilizzata per ottenere effetti antidepressivi
è di 900 mg (fra 600 e 1200) al giorno di estratto secco suddiviso in tre dosi (6, 7).Gli estratti sono in
genere ben tollerati. Effetti collaterali minori (Tabella II) come nausea, rash, astenia, irrequietezza,
sono stati osservati nel corso di studi clinici in una percentuale che va dal 2,4 al 7,4 % (8, 9).Vengono
anche riportati secchezza delle fauci, vertigini e confusione mentale (10).
Per quanto riguarda la fotosensibilità (frequentemente riportata come possibile effetto collaterale),
nell'uomo sono stati documentati solo due casi: uno in un soggetto che ha fatto uso di iperico per 3
anni (11), ed un altro caso che riguarda una donna di 35 anni, che dopo 4 settimane trattamento,
sviluppò una neuropatia non meglio specificata (12). In entrambi i casi i sintomi regredirono in seguito
alla sospensione del trattamento. Altri studi indicano che la fotosensibilità si manifesti con dosaggi più
alti rispetto alla dose consigliata (13).Sono riportati anche effetti avversi gravi (Tabella II) Un paziente
di 20 anni, cui era stata diagnosticata una psicosi maniaco-depressiva e che aveva sostituito la cura
prescritta per il disturbo bipolare con l'iperico alla dose comunemente consigliata di 900 mg/die,
manifestò un episodio caratterizzato da estrema agitazione, irritabilità, ansia e insonnia (14). Una
donna di 51 anni, che a 26 anni aveva avuto un episodio di agitazione di tipo psicotico, cui era
seguito un trattamento con litio e aloperidolo fino all'età di 41 anni senza manifestare ulteriori sintomi
psichiatrici, andò incontro ad agitazione psicomotoria con comportamento bizzarro e linguaggio
disorganizzato (15), dopo alcuni giorni dalla autosomministrazione, su consiglio della sorella, di iperico
(900 mg/die). La sintomatologia è regredita una volta sospeso l'iperico ed iniziata terapia con litio e
2 Acura di Gioacchino Calapai, Giovanni Polimeni, e Achille P. Caputi (2000)
Stress e Sonno 2900.002
aloperidolo. In entrambi i casi sopra riportati la comparsa della sintomatologia è stata messa in relazione con l'assunzione di iperico (14).
Dopo questa prima segnalazione, sono comparsi in letteratura altri tre casi di possibile induzione di mania in relazione all'uso di iperico (15). Una recente revisione della letteratura ha evidenziato che l'incidenza di reazioni avverse in trattamenti a breve-medio termine (2-8 settimane) è più bassa di quella associata ad antidepressivi triciclici (16). Tuttavia gli stessi autori sottolineano come siano ancora insufficienti i dati sul trattamento a lungo termine e come siano inesistenti gli studi sulla teratogenesi, cioè le conoscenze dei possibili effetti dell'iperico nelle donne in gestazione
Sono documentate alcune interazioni tra iperico e farmaci (Tabella III). Sindrome serotoninergica è stata riscontrata in pazienti che hanno associato l'iperico a farmaci antidepressivi quali sertralina, nefazodone (17) e trazodone (18). La sindrome serotoninergica è caratterizzata da alterazione dello stato mentale ed anomalie neuromuscolari quali tremore, aumento dei riflessi tendinei o mioclonie ed è correlata al trattamento con farmaci che aumentano l'attività del sistema serotoninergico (19). Letargia ed incoerenza sono state descritte dopo associazione di paroxetina ed iperico (20).
L'iperico infine determina alterazioni della cinetica di altri farmaci: riduce la concentrazione serica di teofillina (21), digossina (22) e ciclosporina (23), l'AUC della stessa digossina (22) e del fenprocumone (24). Molti studi, ma non tutti, indicano che l'iperico sia un inibitore degli isoenzimi del citocromo P450 (25).
Tabella II. Segnalazioni di reazioni avverse in soggetti in trattamento con Hypericum
perforatum.
Reazione avversa
Referenza bibliografica
Effetti collaterali Nausea, rash, astenia,
Woelk H. et al., J. Geriatr. Psichiatry
Neurol. 1994; 7 (Suppl 1): S34-S38. Schrader E. et al., Hum. Psychopharmacol. 1998; 13: 163-169.
Secchezza delle fauci,
St. John's wort. Med. Lett. Drugs Ther.
vertigini, confusione mentale.
1997; 39: 107-108.
Fotosensibilità
Golsch S. et al., Hautarzt 1997; 48: 249-252. Bove GM et al., Lancet 1998; 352: 1121-1122.
Effetti collaterali Mania
Nierenberg AA et al., Biol. Psichiatry
1999; 46: 1707-1708. Moses EL et al., J Clin Psychopharmacol 2000; 20: 115-117.
Sindrome serotoninergica
Lantz MS et al., J. Geriatr. Psichiatr. Neurol. 1999; 12: 7-10.
Tabella III. Interazioni tra iperico e farmaci, con conseguenze cliniche o
laboratoristiche della interazione.
Conseguenze
Referenza bibliografica
Letargia/incoerenza
Gordon JB. Am Fam Phys. 1998: 57: 950.
Lieve sindrome serotoninergica
Demott K. Clin Psychiatry News 1998: 26; 28.
Stress e Sonno
Lieve sindrome serotoninergica
Lantz et al. J. Geriatr. Psichiatr. Neurol. 1999; 12: 7-10.
Lieve sindrome serotoninergica
Lantz et al. J. Geriatr. Psichiatr. Neurol. 1999; 12: 7-10.
Riduzione della concentrazione
Nebel et al. Ann. Pharmacother 1999; 33: 502.
Riduzione dell'AUC, della
Johne et al. Clin Pharmacol
concentrazione di picco e della
Ther 1999; 66: 338-345.
concentrazione totale
Fenprocumone Riduzione dell'AUC
Maurer et al. Eur J Clin Pharmacol 1999; 55: A22.
Riduzione della concentrazione
Bon et al Schweitzer Apothekerzeitung 1999; 16:535-536.
2900.6.3.8 Bibliografia
Vedi: 2900.6.9.3
Stress e Sonno 2900.002
2900.6.4 LUPPOLO, Humulus lupulus, Canabaceae
2900.6.4.1 Droga
Infiorescenza femminile. RR
PA: OE e altri componenti che agiscono in sinergia.
2900.6.4.2 Punto d'impatto
SNC, SNA, Vie urogenitali, Cute
2900.6.4.3 Proprietà
Amaro-tonica, digestiva, sedativa, ipnotica,
batteriostatica, estrogenica
2900.6.4.4 Indicazioni
Agitazione
Inappetenza nei bambini
Cistiti recidivanti
Depressione lieve
Insonnia d'origine nervosa
Disturbi del sonno nell'adulto e nel
Ipereccitabilità sessuale
Enuresi notturna
Stati di tensione
Eretismo cardiaco
Turbe della menopausa
2900.6.4.5 Posologia
1 o 2 Arkocapsule 2 volte al giorno
2900.6.4.6 Fitovigilanza
Luppolo (Humulus Lupulus)3
Il luppolo è utilizzato da vari secoli per le sue proprietà sedative ed
ipnotiche.
Le sue tradizionali indicazioni sono: nevralgia, insonnia, eccitabilità e
principalmente agitazione associata a tensione nervosa. Così come tutte le
erbe che hanno effetti sedativi (es. kava, valeriana, passiflora), il luppolo
può avere un effetto depressivo additivo quando somministrato con
agenti antipsicotici e benzodiazepine.
A causa delle potenziali conseguenze negative sulla salute, si consiglia
particolare attenzione quando il luppolo viene somministrato insieme a tutti i
farmaci che hanno attività antidepressiva (antidepressivi triciclici e di nuova
generazione), sedativa (alprazolam) ed anticonvulsivante (fenitoina,
fenobarbital, carbamazepina, acido valproico).
L'eccessiva depressione del sistema nervoso centrale si manifesta con sonnolenza, vertigini, alterazione della coordinazione motoria e della concentrazione. In alcuni casi si possono manifestare insufficienze circolatorie ed insufficienze respiratorie talmente gravi da indurre coma o addirittura morte del paziente.
3 a cura di Francesco Salvo, Dipartimento Clinico e Sperimentale di Medicina e Farmacologia, Università degli Studi di Messina, citato solo per onestà intellettuale.
Stress e Sonno
2900.6.4.7 Bibliografia
Vedi: 2900.6.9.4
Stress e Sonno 2900.002
2900.6.5 MELISSA, Melissa officinalis, Lamiaceae
2900.6.5.1 Droga
Foglia. RR
2900.6.5.2 Composizione chimica
Acidi triterpenici, polifenoli e OE
OE. = Essenze triterpeniche: Citrale e Citronellale.
Titolazione minima al 4% dei derivati idrossicinnamici espressi in acido Rosmarinico
2900.6.5.3 Punto d'impatto
SNC, SNA, Apparato digestivo
2900.6.5.4 Proprietà
Sedativa generale, Spasmolitica, Stomachica, Carminativa, Coleretica
2900.6.5.5 Indicazioni
Aerofagia
Disassuefazione al tabacco
Distonia neurovegetativa
Spasmi del tratto gastrointestinale
Dolori di origine nervosa
Fame nervosa
2900.6.5.6 Posologia
1 o 2 Arkocapsule 2 volte al giorno
2900.6.5.7 Fitovigilanza
Nessun effetto indesiderato è stato descritto.
Nessuna interazione con i medicinali è stata riportata.
2900.6.5.8 Bibliografia
Vedi: 2900.6.9.5
Stress e Sonno
2900.6.6 PASSIFLORA, Passiflora incarnata, Passifloraceae
2900.6.6.1 Generalità
Pianta di origine tropicale e subtropicale (Perù e
Brasile).
Coltivata nel sud Europa (Mediteranno).
RR – EMEA.
2900.6.6.2 Droga
Parte aerea. Si dosano i flavonoidi totali (minimo 2%
espressi in Vitexina).
2900.6.6.3 Principi attivi interessanti
2900.6.6.3.1 Alcaloidi
Derivati della carbolina Alcaloidi ipnotici e sedativi: Armano La struttura è molto vicina a quelle delle famigerate benzodiazepine, raffigurata sopra.
2900.6.6.3.2 Flavonoidi
Struttura dei flavonoidi della famiglia della Vitexina:
Azione del totum
La Passiflora ha una spiccata attività ansiolitica, ma tutt'ora non è del tutto chiaro il meccanismo d'azione anche se molti lavori sono stati pubblicati. È un'ultima conferma dell'interesse dell'uso del totum di una droga vegetale.
2900.6.6.4 Punto d'impatto
SNC, Cuore, Apparato digestivo
Stress e Sonno 2900.002
2900.6.6.5 Proprietà
Ansiolitica, Sedativa, Antispasmodica
2900.6.6.6 Studio clinico
È importante ricordare che l'azione neurosedativa è dovuta alla sinergia dei diversi principi attivi della
passiflora (anche in quantità minima). La polvere totale permette e rispetta questa sinergia.
Delaveau ha fatto uno studio clinico in doppio cieco contro l'Oxazepam. La passiflora si è rivelata
altrettanto performante ma con pochissimi effetti secondari.
2900.6.6.7 Indicazioni
Agitazione
Insonnia da stress
Intestino irritabile
Disassuefazione al tabacco
Disassuefazione dai trattamenti con
Disturbi del sonno
Eretismo cardiaco
Risvegli notturni
Insonnia d'origine nervosa
Turbe della menopausa
2900.6.6.8 Posologia
1 o 2 Arkocapsule 2 volte al giorno
2900.6.6.9 Fitovigilanza4
Sono note circa 400 specie della pianta Passiflora. La specie utilizzata in terapia è la Passiflora
incarnata. Originaria del Sud America, possiede effetti sedativi ed attività spasmolitica. Deve il suo
nome, che significa "fiore della passione" ("passion florew" nei paesi di lingua anglosassone), alla
somiglianza della sua corona di petali con una corona di spine. Nella medicina popolare la Passiflora
è stata utilizzata per il trattamento di nevralgie, convulsioni generalizzate, sindromi isteriche,
tachicardia di origine psicogena, asma e insonnia (1). Nella moderna fitoterapia, le indicazioni
terapeutiche si basano su valutazioni di tipo empirico. Viene usata principalmente per il trattamento
dell'ansia e dell'insonnia e, meno frequentemente, per alleviare disturbi gastrointestinali di origine
psicosomatica (2). E' stato pubblicato uno studio clinico che mette in evidenza gli effetti sedativi della
Passiflora, ma esso è stato condotto con preparazioni erboristiche che contengono, insieme alla
Passiflora, altre piante ad azione sedativa (3). In commercio sono presenti associazioni con varie altre
piante. Una delle associazioni più frequenti è quella con la valeriana (4).
Tra i costituenti chimici attivi vi sono glicosidi, flavonoidi, maltolo e alcaloidi (5, 6, 7, 8). Non è chiaro
quale o quali tra i costituenti siano i responsabili degli effetti della Passiflora ed è probabile che, come
avviene per moltissime piante medicinali, essi siano il risultato di un'azione sinergica tra le diverse
sostanze contenute (1, 2, 4, 9).
Le parti della pianta usate sono costituite dalle parti aeree. Può essere assunta sotto forma di infuso,
tintura, compresse o polvere di pianta. Per quanto riguarda il dosaggio viene utilizzata negli adulti la
dose di 0,5-2 g o 1-4 ml di tintura per 3-4 volte al giorno (10
EFFETTI COLLATERALI Sonnolenza o eccessiva sedazione. CONTROINDICAZIONI Uso concomitante di alcool o di benzodiazepine (possibile potenziamento della sedazione). REAZIONI AVVERSE
4 A cura di Gioacchino Calapai, Giovanni Polimeni, e Achille P. Caputi
Stress e Sonno
Dopo assunzione di Passiflora è stato segnalato un caso di vasculite cutanea associata ad orticaria
(11). Sono stati segnalati 5 casi di pazienti che, dopo avere assunto preparazioni a base di Passiflora, hanno riportato uno stato di alterazione della coscienza tale da richiedere la ospedalizzazione (12). Asma associata a rinite è stata diagnosticata in un soggetto che per motivi professionali (lavorava in farmacia) era stato esposto a materiale a base di estratto di Passiflora del tipo alata (13). Recentemente è stato segnalato il caso di una donna di 34 anni che in seguito ad ingestione di Passiflora incarnata (3,5 grammi in 2 giorni), assunta per curare una forma di stress, ha presentato nausea, vomito, sonnolenza, alterazioni elettrocardiografiche (aumento dell'intervallo QT e aritmia ventricolare). Le cause che hanno scatenato l'episodio non sono state chiarite. Per tale motivo è stata fatta l'ipotesi che la donna fosse portatrice di una variazione genetica a carico del citocromo 450 tale da causare una riduzione del metabolismo dei principi attivi presenti nella pianta che potrebbero poi aver raggiunto livelli tossici (14)
2900.6.6.10 Bibliografia
Vedi: 2900.6.9.6
Stress e Sonno 2900.002
2900.6.7 RODIOLA,
Rhodiola rosea,
Pianta d'origine siberiana. La Rodiola è una pianta adattogena.
2900.6.7.1 Droga
Radice di piante di almeno 4 anni.
La radice emana un odore simile a quello della rosa, di cui il nome
"rosea".
Attenzione, la Rodiola non è facilmente reperibile e sono spesso
proposte delle piante simili prive di azione fisiologica o farmacologica.
2900.6.7.2 Principi attivi
L'identificazione certa della pianta avviene con la riconoscenza di 3 principi attivi: i rodiolosidi.
Rosina+Rosavina +Rosarina :
0,497%,cv 42% , max 0,825% - min 0,198%
Gli altri principi attivi come il Salidroside e il Tirosolo non sono
caratteristici di questa pianta.
Non sono disponibili tuttora metodi di dosaggio standard delle
Rovasina, Rosina e Rosarina.
Nessun testo ufficiale (Farmacopea o Escop) è mai stato pubblicato al
riguardo.
2900.6.7.3 Punto d'impatto
SNC, Cuore, Sistema immunitario, Adipociti
2900.6.7.4 Proprietà
Antistress, Adattogeno, Tonico
2900.6.7.5 Indicazioni
Affaticamento intellettivo
Fame nervosa
Insonnia da stress
Depressione leggera
Depressione reattiva
Disassuefazione al tabacco
Stanchezza fisica
Disturbi del sonno
Stati di tensione
Disturbi della funzione erettile
Stress passeggero
Esaurimento nervoso
2900.6.7.6 Posologia
1 o 2 Arkocapsule 2 volte al giorno
Stress e Sonno
2900.6.7.7 Fitovigilanza5
La rhodiola (Rhodiola rosea) è una pianta ampiamente diffusa nelle regioni artiche e montuose
dell'Europa e dell'Asia (1). Grazie alle sue proprietà adattogene (aumenta la resistenza e la capacità di
adattamento dell'organismo agli agenti stressanti), trova impiego come antistress, antiossidante ed
immunostimolante, nel trattamento del senso di affaticamento e come stimolante della memoria (2,3).
Gli estratti della pianta sono anche stati studiati come antiaritmici, cardioprotettivi e antitumorali (4). I
principali composti chimici, presenti nella rhodiola e responsabili della sua attività biologica,
includono: salidrosina, tirosolo, rosavina, rosarina e rosina (5).
Un recente studio in vitro ha dimostrato una potente attività inibente della rhodiola nei confronti del
CYP3A4 e della glicoproteina-P (6). Sebbene questo effetto non sia stato ancora confermato
nell'uomo, ai pazienti in trattamento con farmaci come warfarin (substrato del CYP3A4) o digossina
(substrato della glicoproteina-P) viene suggerito di evitare l'uso concomitante di prodotti a base di
rhodiola.
2900.6.7.8 Effetti collaterali:
Il sovradosaggio di Rodiola può provocare irritabilità, eccitabilità, tremori alle mani e tic nervosi. Può
peggiorare un'insonnia preesistente.
2900.6.7.9 Controindicazioni:
Non è consigliabile in gravidanza e durante l'allattamento a causa della mancanza di dati clinici.
2900.6.7.10 Bibliografia
Vedi: 2900.6.9.7
5 (a cura di Alessandro Oteri, Dipartimento Clinico e Sperimentale di Medicina e Farmacologia, Università degli Studi di Messina)
Stress e Sonno 2900.002
2900.6.8 VALERIANA, Valeriana officinalis,
Valerianaceae
Iscritta nella farmacopea Italiana X Ed., farmacopea europea IV Ed. e
ESCOP. La radice (valere in latino significa essere forte e in buona salute)
contiene degli oli essenziali e dell'acido valerianico che hanno entrambi
un'azione sedativa. Esistono testi da più di 2000 anni che menzionano l'uso
della valeriana: è stata la droga vegetale più usata fino all'arrivo dei
tranquillanti e sonniferi chimici. Dal 1980, la Valeriana è stata reintrodotta
nei trattamenti dell'insonnia e dell'ansia. RR EMEA.
2900.6.8.1 Origine
La specie officinalis è comune in tutta l'Europa (salvo nel Mediterraneo). La
valeriana cresce in zone umide. La droga usata proviene soprattutto da culture (Francia, Germania o
paesi dell'est).
2900.6.8.2 Droga
Organi sotterranei: radice, stoloni.
La radice della Valeriana ha un odore particolare e caratteristico (pipì di gatto).
Deve contenere un minimo di 0.5% in OE.
PA: Titolate allo 0,17% minima d'Acidi Sesquiterpinici (espressi in acido Valerenico) e allo 0,3% (V/m)
in Oli essenziali.
Numerosi costituenti della pianta sono stati isolati e identificati.
Stress e Sonno
2900.6.8.3 Punto d'impatto
SNC, SNA, Apparato digestivo, Fegato, sangue
Azione sedativa e ipnotica dell'acido valerenico e dei valepotriati sul SNC.
Diminuisce il colesterolo totale nel sangue e LDl colesterolo.
2900.6.8.4 Proprietà
Ansiolitica, Sedativa, Ipnotica, Spasmolitica.
2900.6.8.5 Meccanismo d'azione
MENNINI e al. 1993; SANTOS et al. 1994a, 1994b hanno messo in evidenza il ruolo dell'acido
Valerenico nell'inibizione della degradazione del GABA.
Stress e Sonno 2900.002
Acido Valerenico
- Inibizione
GABA Degradato
[GABA] circolante
2900.6.8.6 Osservazioni sull'uomo
La maggioranza degli studi riguarda il sonno.
Miglioramento significativo su 126 pazienti insonni e nevrotici, azione ottenuta con una miscela di
valepotriati.
L'effetto ansiolitico è stato paragonato quello del diazepam.
Prove fatte in Germania e Messico hanno evidenziato una riduzione significativa del tempo di
addormentamento ed un miglioramento della qualità del sonno.
Molte associazioni con altre piante si sono dimostrate attive: Luppolo, Kava kava, Iperico,
Biancospino.
2900.6.8.7 Indicazioni
Affaticamento intellettivo
Ansia
Cefalea
Difficoltà all'addormentamento
Disassuefazione dal tabacco
Disturbi del sonno
Emicrania
Insonnia
Insonnia d'origine nervosa
Insonnia da stress
Ipereccitabilità
Nervosismo
Risvegli notturni
Spasmi gastrici
Stati di tensione
Stress
Turbe della menopausa
Stress e Sonno
2900.6.8.8 Posologia
1 o 2 Arkocapsule 2 volte al giorno
2900.6.8.9 Effeti collaterali e tossicità
La tossicità della valeriana è bassissima: DL50 dell'estratto (topino,I.P.) : 360-400 mg/kg; per os.
Non interferisce con gli altri depressori del SNC : diazepam, aloperinolo…)
È una delle piante che interferisce meno con l'attività dei citocromi (debole su CYP3A4, nulla su
CYP2D6)
2900.6.8.10 Fitovigilanza
Interazioni con i farmaci6
La valeriana (Valeriana officinalis) viene comunemente utilizzata per il trattamento dell'insonnia e come spasmolitico a livello gastrointestinale. Applicazioni di minore importanza comprendono il trattamento dei crampi muscolari e uterini, della cefalea e l'utilizzo come carminativo a livello gastrointestinale.
L'effetto sedativo è dovuto ai valepotriati, principi attivi presenti nell'olio essenziale, che inducono un rilascio dose dipendente del GABA ed un'inibizione dell'enzima che metabolizza tale neurotrasmettitore (1-3). Da studi in vitro, sembra che la valeriana abbia la capacità di inibire l'isoforma CYP3A4 del citocromo P450, in maniera variabile da lieve a moderata (35-88%). Non è comunque noto se questo si verifichi anche in vivo(4). L'uso concomitante della valeriana e di agenti epatotossici può determinare un incremento del rischio di epatotossicità. L'effetto si presenta anche quando viene associata ad altre erbe dotate di potenziale epatotossico (5). In letteratura sono riportati quattro casi di epatotossicità in altrettanti pazienti che avevano assunto la valeriana insieme alla scutellaria (Scutellaria baicalensis). Al momento dell'insorgenza dei sintomi, la durata della terapia con le due erbe variava da tre giorni a due mesi. Tre pazienti avevano urine scure e feci acoliche, e tutti e quattro i pazienti presentavano ittero. Dopo la sospensione delle due erbe, i valori ritornarono nella norma in tutti e quattro i pazienti nel giro di due anni (6).
Numerose altre erbe medicinali non dovrebbero essere assunte insieme alla valeriana per lo stesso motivo (tra cui Larrea tridentata, Symphytum x uplandicum, Tussilago farfara, Teucrium chamaedrys, jin bu huan, Piper methysticum, Mentha pulegium, Hedeoma pulegoides, Petasites japonicus) (5). Nel caso di assunzione contemporanea di valeriana e di agenti epatotossici, si raccomanda quindi di monitorare i possibili segni o sintomi di epatotossicità.
La somministrazione concomitante di valeriana e di benzodiazepine o barbiturici può determinare
un incremento della depressione del SNC o la riduzione dell'efficacia di tali farmaci. Gli estratti di
valeriana, infatti, sono dotati di affinità per i recettori centrali e periferici delle benzodiazepine e dei
barbiturici oltre che dei recettori GABA-A (7). In altri casi, la valeriana ha dimostrato di poter sostituirsi
alle benzodiazepine spiazzandole dal loro legame recettoriale, ed in tal modo riducendone l'effetto (8).
Nei topi, l'uso di valeriana incrementa il sonno indotto dal pentobarbital e l'anestesia indotta dal
tiopental (9-11). L'assunzione contemporanea di valeriana e analgesici oppioidi può aumentare il loro
effetto sedativo. Tale effetto, osservato finora a livello sperimentale, potrebbe causare anche
depressione respiratoria. Si sconsiglia pertanto tale associazione (12). Associando valeriana ad
etanolo, può verificarsi un rapido incremento della sedazione, di moderata entità. Un case report
riporta un'interazione tra valeriana, ginkgo ed etanolo (13).
6 A cura di Alessandro Oteri e Francesco Salvo, Dipartimento Clinico e Sperimentale di Medicina e Farmacologia, Università degli Studi di Messina
I pazienti che assumono farmaci quali antidepressivi triciclici, litio, inibitori delle MAO, rilassanti muscolo scheletrici, SSRI (per es. duloxetina o venlafaxina) dovrebbero consultare il proprio medico di famiglia prima di assumere valeriana (14).
Anche se non dimostrato con certezza, la valeriana associata alla loperamide può causare delirio
con confusione, agitazione e disorientamento. In letteratura è riportato il caso di delirio in un paziente
che assumeva contemporaneamente valeriana, iperico e loperamide (15). Sebbene non sia noto se e
quali dei tre farmaci abbiano interagito, gli autori del case report consigliano prudenza nel prescrivere
insieme valeriana e loperamide.
2900.6.8.11
Uso della Valeriana nei disturbi del sonno7
L'insonnia è un problema di salute molto diffuso nella popolazione generale. In genere, tale disturbo viene trattato con farmaci di sintesi quali le benzodiazepine o altri ipnotici non benzodiazepinici.
La Valeriana officinalis rappresenta un'alternativa terapeutica con un profilo di sicurezza buono. L'effetto sedativo e ipnoinducente della Valeriana officinalis è noto in Europa sin dal 18° secolo. La sua azione sembra essere determinata da un effetto di inibizione sui neuroni del sistema nervoso simpatico, mediata dal neurotrasmettitore GABA.
Recentemente è stata pubblicata sulla rivista scientifica Sleep Medicine, una metanalisi (tecnica clinico-statistica che permette di analizzare una serie di studi condotti sullo stesso argomento) della letteratura scientifica che valuta l'efficacia della Valeriana officinalis nell'insonnia. Sono stati analizzati complessivamente 18 studi clinici randomizzati e controllati (RCT) per un numero complessivo di 1317 pazienti.
Agli studi è stata applicata la Scala di Jadad, strumento che serve a valutare la qualità e l'adeguatezza metodologica di un RCT. Lo score totale può variare da 0 a 5 e si considera di buona qualità un RCT che ottenga un punteggio >3. Degli studi selezionati 8 raggiungevano un punteggio di 5.
Sono stati valutati i seguenti parametri (outcome): miglioramento della qualità del sonno e tempo di latenza prima di prendere sonno, misurato in minuti.
Non si sono registrate differenze significative nel tempo di addormentamento dei soggetti trattati con Valeriana officinalis rispetto a quelli trattati con placebo. Questo dato è in accordo con studi precedenti che hanno ripetutamente dimostrato che la Valeriana officinalis non ha un reale effetto sul tempo di latenza prima del sonno.
Al contrario, la metanalisi ha messo in luce che l'estratto di radice di Valeriana officinalis a dosi che vanno da 300 a 600 mg al giorno è in grado di migliorare la qualità del sonno. In particolare lo studio sottolinea come i soggetti che assumono Valeriana officinalis, alle dosi sopraindicate, abbiano la percezione di un sonno qualitativamente migliore e, conseguentemente, ottengano un miglioramento soggettivo dell'insonnia.
Nonostante i limiti dell'efficacia, la scarsità degli effetti collaterali suggerisce che l'uso della Valeriana officinalis nei lievi disturbi del sonno produce più benefici che rischi.
7 A cura di Antonio Carnì, Medico Ambulatorio di Medicina Naturale AOU-Policlinico "G.Martino"-Messina
Estratto da: Fernández-San-Martín MI, Masa-Font R, Palacios-Soler L, Sancho-Gómez P, Calbó-Caldentey C, Flores-Mateo G. Effectiveness of Valerian on insomnia: a meta-analysis of randomized placebo-controlled trials. Sleep Med 2010; 11: 505-11.
2900.6.8.12
Programma per smettere di fumare
Lottare contro la sindrome di astinenza alla nicotina
NoTa Bene:
La Nicotina del tabacco crea una dipendenza fisica e psicologica importante. Quando si vuole smettere di fumare, il soggetto va incontro ad una vera sindrome di astinenza. È importante sostenere queste persone durante il periodo di disassuefazione. Arkopharma, un metodo efficace, provato, sicuro e facile: l'uso della fitoterapia.
Dispositivo Medico CE
2900.6.8.12.2 NTB
NTB si presenta sotto forma di sigarette che contengono foglie di Papaia, di Nocciolo e di Menta. Non
contengono nicotina. Il principio è di favore la gestualità del fumatore che ha bisogno di accendere
una sigaretta ma non trova il piacere di fumare, come nel caso delle vere sigarette. Alla lunga, l'ex
fumatore perde anche la voglia fisica di accendere la sua sigaretta.
Dal punto di vista tossicologico, le sigarette NTB, 2 studi hanno dimostrato di non creare problemi a
livello cardio-vascolare. NTB contiene circa un terzo di CO, Acroleina e condensato, e soprattutto
NON CONTIENE NICOTINA.
Le Arkocapsule della linea Blu possono aiutare ad un consiglio più personalizzato in base al
problema che incontra la persona desiderosa di smettere di fumare. Per far fronte alla maggiore parte
dei problemi è sempre consigliabile la Valeriana Arkocapsule. In genere 2 capsule mattina e sera.
Si possono anche consigliare delle associazioni, come indicato nella tabella qui sotto.
2900.6.8.13 Bibliografia
Vedi: 2900.6.9.8
2900.6.9 Bibliografia Linea Blu
2900.6.9.1 Biancospino
Wagner H, Tittel G, Bladt S. Analyse und Standardisierung von Arzneidrogen und Phytopräparaten durch
Hochleistungsflüssig-chromatographie (HPLC) und andere chromatographische Verfahren 1. Mitteilung : Flavonoiddrogen.
Dtsch Apoth Ztg 1983;123:515-21.
Ficarra P, Ficarra R, Tommasini A, De Pasquale A, Guarniera Fenech C, Iauk L. High-performance liquid chromatography
of flavonoids in Crataegus oxyacantha L. Farmaco [Prat] 1984;39:148-57.
Pietta P, Manera E, Ceva P. Isocratic liquid chromatographic method for the simultaneous determination of Passiflora
incarnata L. and Crataegus monogyna flavonoids in drugs. J Chromatogr 1986;357:233-8.
Nikolov N, Seligmann O, Wagner H, Horowitz RM, Gentili B. Neue Flavanoid-Glycoside aus Crataegus monogyna und
Crataegus pentagyna. Planta Med 1982;44:50-3.
Wagner H, Grevel J. Herzwirksame Drogen IV. Kardiotone amine aus Crataegus oxyacantha. Planta Med 1982;45:98-101.
Beretz A, Haag-Berrurier M, Anton R. Choix de méthodes pharmacologiques pour l'étude des activités de l'aubépine. Plantes
Méd Phytothér 1978;12:305-14.
Ammon HP, Handel M. Crataegus, Toxicologie und Pharmakologie. Planta Med 1981;43(1):105-20;(2):209-39;(3): 313-22.
Paris M. L'aubépine, Crataegus oxyacantha L. (Rosacées). Phytotherapy 1983;6:5-10.
Totte J, Vlietinck AJ. Produits phytothérapeutiques et système cardiovasculaire. J Pharm Belg 1986;41:330-61.
Costa R, Occhiuto F, Circosta C, Ragusa S, Busa G, Briguglio F, Trovato A. Etude comparée de l'activité cardiovasculaire
des pousses des feuilles et des fleurs de Crataegus oxyacantha II. Action de préparations extractives et de principes actifs
purs isolés sur le coeur isolé de Lapin. Plantes Méd Phytothér 1986;20:52-63.
Costa R, Occhiuto F, Circosta C, Ragusa S, Busa G, Briguglio F, Trovato A. Etude comparée de l'activité cardiovasculaire
des pousses des feuilles et des fleurs de Crataegus oxyacantha III. Action protectrice sur le coeur isolé de Rat vis-à-vis des
agents arythmo-gènes et dans les arythmies par reperfusions. Plantes Méd Phytothér 1986;20:115-28.
Lievre M, Andrieu J-L, Baconin A. Etude des effets cardiovasculaires de l'hypéroside extrait de l'aubépine chez le Chien
anesthésié. Ann Pharm Fr 1985;43:471-7.
Occhiuto F, Circosta C, Briguglio F, Tomasini A, De Pasquale A. Etude comparée de l'activité cardiovasculaire des
pousses des feuilles et des fleurs de Crataegus oxyacantha I. Activité électrique et tension artérielle chez le Rat. Plantes Méd
Phytothér 1986;20:37-51.
Lacaille-Dubois, Franck U, Wagner H. Search for potential angiotensin converting enzyme (ACE)-inhibitors from plants.
Phytomedicine. 2001 Jan;8(1):47-52.
Bahorun T, Trotin F, Pommery J, Vasseur J, Pinkas M. Antioxidant activities of Crataegus monogyna extracts. Planta Med.
1994 Aug;60(4):323-8.
Bahorun T, Aumjaud E, Ramphul H, Rycha M, Luximon-Ramma A, Trotin F, Aruoma OI. Phenolic constituents and
antioxidant capacities of Crataegus monogyna (Hawthorn) callus extracts. Nahrung 2003 Jun;47(3):191-8.
Ahumada C, Saenz T, Garcia D, De La Puerta R, Fernandez A, Martinez E. The effects of a triterpene fraction isolated from
Crataegus monogyna Jacq. On different acute inflammation models in rats and mice. Leucocyte migration and phospholipase
A2 inhibition. J Pharm Pharmacol 1997;49(3):329-31.
Saenz MT, Ahumada MC, Garcia MD. Extracts from Viscum and Crataegus are cytotoxic against larynx cancer cells. Z
Naturforsch [C]. 1997;52(1-2):42-4.
Fong HH, Bauman JL. Hawthorn. J Cardiovasc Nurs 2002 Jul;16(4):1-8.
Iwamoto M, Ishizaki T, Sato T. Klinishe wirchung von Crataegutt bei Herzerkrankungen ischämischer und/oder hypertensiver
Genese. Eine multizentrische Doppelblindstudie. Planta Med 1981;42:1-16.
Tauchert M. Efficacy and safety of crataegus extract WS 1442 in comparison with placebo in patients with chronic stable New
York Heart Association class-III heart failure. Am Heart J 2002;143(5):910-5.
Hanus M, Lafon J, Mathieu M. Double-blind, randomised, placebo-controlled study to evaluate the efficacy and safety of a
fixed combination containing two plant extracts (Crataegus oxyacantha and Eschscholtzia californica) and magnesium in mild-
to-moderate anxiety disorders. Curr Med Res Opin 2004 20(1):63-71.
Delaveau P. L'aubépine. Le Concours Médical 1984;106:1323-4.
Aubépine, dossier toxicologique. Travaux des Laboratoires ARKOPHARMA.
2900.6.9.2 Escolzia
Eschscholtzia californica pour préparations homéopathiques. Pharmacopée française, Xème éd., janvier 1989.
Guedon D, Cappelaere N, Simaner V. HPLC analysis of the main alkaloids from Eschscholtzia californica Cham. Travaux des
laboratoires Arkopharma.
Beck MA, Haberlein H. Flavonol glycosides from Eschscholtzia californica. Phytochemistry 1999;50(2):329-32.
Delaveau P. Eschscholtzia de Californie. Actual Pharm 1984;208:33-4.
Preininger V. Chemotaxonomy of Papaveraceae and Fumariaceae. In : The alkaloids, A. Brossi éd., Londres, Academic Press
1986;29:1-98.
Slavik J, Slavikova I. On alkaloid from aerial parts of three Eschscholtzia species. Collect Czech Chem Commun
1986;51:1743-51.
Fabre N, Claparols C, Richelme S, Angelin ML, Fouraste I, Moulis C. Direct characterization of isoquinoline alkaloids in a
crude plant extract by ion-pair liquid chromatography-electrospray ionization tandem mass spectrometry: example of
Eschscholtzia californica. J Chromatogr A 2000;904(1):35-46.
Gözler B, Lantz MS, Shamma M. The pavine and isopavine alkaloids. J Nat Prod 1983;46:293-309.
Maschi P. Etude analytique par méthodes chromatographiques d'extraits d'Eschscholtzia californica. DESS de Contrôle des
Médicaments, Châtenay Malabry, 1983.
Üstünes L, Laekeman GM, Gözler B, Vlietinck AJ, Özer A, Herman AG. In vitro study of the anti-cholinergic and
antihistaminic activities of protopine and some derivatives. J Nat Prod 1988;51:1021-2.
Kardos J, Blasko G, Simonyi M. Enhancement of g-aminobutyric acid redeptor binding by protopine type alkaloids.
Arzneimittelforschung 1986;36:939-40.
Simanek V. Benzophenanthridine alkaloids. In : The alkaloids, A. Brossi éd., Londres, Academic Press 1985;26:185-240.
Becci PJ, Schwartz H, Barnes HH, Lee Southard G. Short-term toxicity studies of sanguinarine and of two alkaloid extracts
of Sanguinaria canadensis L. J Toxicol Environ Health 1987;20:199-208. Pour une bibliographie complète se reporter à A.
Brossi , op. cit., ainsi qu'aux revues périodiques de K.W. Bentley : b-phenylethylamines and the isoquinoline alkaloids. Nat
Prod Rep depuis 1984 jusqu'à 2005 : Nat Prod Rep 1984;1:355-70; 1985;2:81-96; 1986;3:153-69; 1987;4:677-702;
1988;5:265- 92 ;. 2004;21:395-424 ; 2005;22:249-68.
Rolland A, Fleurentin J, Lanhers MC, Younos C, Misslin R, Mortier F, Pelt JM. Behavioural effects of the American
traditional plant Eschscholzia californica: sedative and anxiolytic properties. Planta Med 1991;57(3):212-6.
Vincieri FF, Celli S, Mulinacci N, Speroni E. An approach to the study of the biological activity of Eschscholtzia californica.
Pharmacol Res Commun 1988;20:41-4.
BaldaccI R. Contribution à l'utilisation en médecine de ville d'Eschscholtzia californica. Phytotherapy 1984;9:31-2.
Hanus M, Lafon J, Mathieu M. Double-blind, randomised, placebo-controlled study to evaluate the efficacy and safety of a
fixed combination containing two plant extracts (Crataegus oxyacantha and Eschscholtzia californica) and magnesium in mild-
to-moderate anxiety disorders. Curr Med Res Opin 2004;20(1):63-71.
Kleber E, Schneider W, Schafer HL, Elstner EF. Modulation of key reactions of the catecholamine metabolism by extracts
from Eschscholtzia californica and Corydalis cava. Arzneimittelforschung 1995;45(2):127-31. (b) Blechert S, Brodschelm W,
Holder S, Kammerer L, Kutchan TM, Mueller MJ, Xia ZQ, Zenk MH. The octadecanoic pathway: signal molecules for the
regulation of secondary pathways. Proc Natl Acad Sci U S A. 1995;92(10):4099-105.
Schafer HL, Schafer H, Schneider W, Elstner EF. Sedative action of extract combinations of Eschscholtzia californica and
Corydalis cava. Arzneimittelforschung 1995;45(2):124-6.
Escholtzia, dossier toxicologique. Travaux des laboratoires Arkopharma.
2900.6.9.3 Iperico
2900.6.9.3.1 Bibliografia
generale
Hobbs C, St. John's wort, Herbal Gram, 1988, 24-33.
Karriev M.O., Phytochemical study of Hypericum plants of the Turkemenian flora, Izv Akad Nauk
SSR 1980;52-57.
Nahrstedt A, Butterweck V. Biologically active and other chemical constituents of the herb of
Hypericum perforatum L. Pharmacopsychiatry 1997;30 Suppl 2:129-34.
Chialva F. et al, Study of the composition of essential oil from Hypericum perforatum L. Riv Ital
EPPOS 1981;63:286-8.
Saljic J. Ointment for the traitment of burns. Ger Offen 1974;2:406-52.
Benedi J, Arroyo R, Romero C, Martin-Aragon S, Villar AM. Antioxidant properties and protective
effects of a standardized extract of Hypericum perforatum on hydrogen peroxide-induced oxidative
damage in PC12 cells. Life Sci 2004;75(10):1263-76.
Silva BA, Dias AC, Ferreres F, Malva JO, Oliveira CR. Neuroprotective effect of H. perforatum
extracts on beta-amyloid-induced neurotoxicity. Neurotox Res 2004;6(2):119-30.
Lu YH, Du CB, Liu JW, Hong W, Wei DZ. Neuroprotective effects of Hypericum perforatum on
trauma induced by hydrogen peroxide in PC12 cells. Am J Chin Med 2004;32(3):397-405.
Zou Y, Lu Y, Wei D. Hypocholesterolemic effects of a flavonoid-rich extract of Hypericum perforatum
L. in rats fed a cholesterol-rich diet. J Agric Food Chem 2005;53(7):2462-6
Gilani AH, Khan AU, Subhan F, Khan M. Antispasmodic and bronchodilator activities of St John's
wort are putatively mediated through dual inhibition of calcium influx and phosphodiesterase. Fundam
Clin Pharmacol 2005;19(6):695-705.
Bukhari IA, Dar A, Khan RA. Antinociceptive activity of methanolic extracts of St. John's Wort
(Hypericum perforatum) preparation. Pak J Pharm Sci 2004;17(2):13-9.
Hölzl J. Inhaltsstoffe und wirkmechanismen des Johanniskrautes. Z Phytother 1993;14:255-64.
Abdel-Salam OM. Anti-inflammatory, antinociceptive, and gastric effects of Hypericum perforatum in
rats. Scientific World Journal 2005;5:586-95.
Menegazzi M, Di Paola R, Mazzon E, Muia C, Genovese T, Crisafulli C, Suzuki H, Cuzzocrea S.
Hypericum perforatum attenuates the development of carrageenan- induced lung injury in mice. Free
Radic Biol Med 2006;40(5):740-53.
Genovese T, Mazzon E, Di Paola R, Muia C, Crisafulli C, Menegazzi M, Malleo G, Suzuki H,
Cuzzocrea S. Hypericum perforatum attenuates the development of cerulein-induced acute
pancreatitis in mice. Shock 2006;25(2):161-7.
Genovese T, Mazzon E, Menegazzi M, Di Paola R, Muia C, Crisafulli C, Bramanti P, Suzuki H,
Cuzzocrea S. Neuroprotection and enhanced recovery with hypericum perforatum extract after
experimental spinal cord injury in mice. Shock 2006;25(6):608-17.
Voss A, Verweij PE. Antibacterial activity of hyperforin from St John's wort. Lancet
1999;354(9180):777.
Perfumi M, Mattioli L, Forti L, Massi M, Ciccocioppo R. Effect of Hypericum perforatum CO2
extract on the motivational properties of ethanol in alcohol-preferring rats. Alcohol 2005;40(4):291-6.
Schempp CM, Kiss J, Kirkin V, Averbeck M, Simon-Haarhaus B, Kremer B, Termeer CC,
Sleeman J, Simon JC. Hyperforin acts as an angiogenesis inhibitor. Planta Med 2005;71(11):999-
1004.
Skalkos D, Stavropoulos NE, Tsimaris I, Gioti E, Stalikas CD, Nseyo UO, Ioachim E, Agnantis
NJ. The lipophilic extract of Hypericum perforatum exerts significant cytotoxic activity against T24 and
NBT-II urinary bladder tumor cells. Planta Med 2005;71(11):1030-5.
Lavie G, Valentine F, Levin B, Mazur Y, Gallo G, Lavie D, Weiner D, Meruelo D. Studies of the
mechanisms of action of the antiretroviral agents hypericin and pseudohypericin. Proc Natl Acad Sci
U S A 1989;86(15):5963-7.
Taher MM, Lammering GM, Hershey CM, Valerie KC. Mood-enhancing antidepressant St. John's
wort inhibits the activation of human immunodeficiency virus gene expression by ultraviolet light.
IUBMB Life 2002;54(6):357-64.
Suzuki O, Katsumata Y, Oya M, Bladt S, Wagner H. Inhibition of monoamine oxidase by hypericin.
Planta Med 1984;50(3):272-4.
Laakmann G, Schule C, Baghai T, Kieser M. St. John's wort in mild to moderate depression: the
relevance of hyperforin for the clinical efficacy. Pharmacopsychiatry 1998;31 Suppl 1:54-9.
Zanoli P. Role of hyperforin in the pharmacological activities of St. John's Wort. CNS Drug Rev
2004;10(3):203-18
Butterweck V. Mechanism of action of St John's wort in depression : what is known? CNS Drugs
2003;17(8):539-62.
Bladt S, Wagner H. Inhibition of MAO by fractions and constituents of hypericum extract. J Geriatr
Psychiatry Neurol 1994;7 Suppl 1:S57-9.
Butterweck V, Hegger M, Winterhoff H. Flavonoids of St. John's Wort reduce HPA axis function in
the rat. Planta Med 2004;70(10):1008-11.
Cott JM. In vitro receptor binding and enzyme inhibition by Hypericum perforatum extract.
Pharmacopsychiatry 1997;30 Suppl 2:108-12.
Hirano K, Kato Y, Uchida S, Sugimoto Y, Yamada J, Umegaki K, Yamada S. Effects of oral
administration of extracts of Hypericum perforatum (St John's
wort) on brain serotonin transporter, serotonin uptake and behaviour in mice. J Pharm Pharmacol
2004;56(12):1589-95.
Bach-Rojecky L, Kalodjera Z, Samarzija I. The antidepressant activity of Hypericum perforatum L.
measured by two experimental methods on mice. Acta Pharm 2004;54(2):157-62.
Trofimiuk E, Walesiuk A, Braszko JJ. St John's wort (Hypericum perforatum) diminishes cognitive
impairment caused by the chronic restraint stress in rats. Pharmacol Res 2005;51(3):239-46.
Schule C, Baghai T, Sauer N, Laakmann G. Endocrinological effects of highdose Hypericum
perforatum extract WS 5570 in healthy subjects. Neuropsychobiology 2004;49(2):58-63.
Schulz H., Jobert M., Der Einfuss von Johanniskraul Extrakt auf das Schlal- EEG Doppelblind
versucht mit Propanden, Nerveilheinkunde 1993;12:323-7.
Holzl J. Johanniskraut- eine alte Arzneipflanze mit neuer bedeutung, Therapeutikon 1989;3:540-7.
Harrer G, Sommer H. Treatment of mild/moderate depressions with hypericum. Phytomedicine
1994a;1:3-8. et Sommer H, Harrer G. Placebo-controlled double-blind study examining the
effectiveness of an hypericum preparation in 105 mildly depressed patients. J Geriatr Psychiatry
Neurol 1994;7 Suppl 1:S9-11.
Schrader E, Meier B, Brattström A. Hypericum treatment of mild-moderate depression in a placebo-
controlled study. A prospective, double-blind, randomized, placebo-controlled, multicentre study. Hum
Psychopharmacol 1998;13:163-9.
Lecrubier Y, Clerc G, Didi R, Kieser M. Efficacy of St. John's wort extract WS 5570 in major
depression: a double-blind, placebo-controlled trial. Am J Psychiatry 2002;159(8):1361-6.
Uebelhack R, Gruenwald J, Graubaum HJ, Busch R. Efficacy and tolerability of Hypericum extract
STW 3-VI in patients with moderate depression: a double-blind, randomized, placebo-controlled
clinical trial. Adv Ther 2004;21(4):265-75.
Harrer G, Hubner WD, Podzuweit H. Effectiveness and tolerance of the hypericum extract LI 160
compared to maprotiline: a multicenter double-blind study. J Geriatr Psychiatry Neurol 1994;7 Suppl
1:S24-8.
Harrer G, Schmidt U, Kuhn U, Biller A. Comparison of equivalence between the St. John's wort
extract LoHyp-57 and fluoxetine. Arzneimittelforschung 1999;49(4):289-96.
Philipp M, Kohnen R, Hiller KO. Hypericum extract versus imipramine or placebo in patients with
moderate depression: randomised multicentre study of treatment for eight weeks. BMJ
1999;319(7224):1534-8.
Schrader E. Equivalence of St John's wort extract (Ze 117) and fluoxetine: a randomized, controlled
study in mild-moderate depression. Int Clin Psychopharmacol 2000;15(2):61-8.
Woelk H. Comparison of St John's wort and imipramine for treating depression: randomised
controlled trial. BMJ 2000;321(7260):536-9.
Behnke K, Jensen GS, Graubaum HJ, Gruenwald J. Hypericum perforatum versus fluoxetine in the
treatment of mild to moderate depression. Adv Ther 2002;19(1):43-52.
Bjerkenstedt L, Edman GV, Alken RG, Mannel M. Hypericum extract LI 160 and fluoxetine in mild
to moderate depression: a randomized, placebo-controlled multi-center study in outpatients. Eur Arch
Psychiatry Clin Neurosci 2005;255(1):40-7.
(a) Gastpar M, Singer A, Zeller K. Efficacy and tolerability of Hypericum extract STW3 in long-term
treatment with a once-daily dosage in comparison with sertraline. Pharmacopsychiatry 2005;
38(2):78-86.
(b) Gastpar M, Singer A, Zeller K. Comparative efficacy and safety of a once-daily dosage of
Hypericum extract STW3-VI and citalopram in patients with moderate depression: a double- blind,
randomised, multicentre, placebo-controlled study. Pharmacopsychiatry 2006;39(2):66-75.
Szegedi A, Kohnen R, Dienel A, Kieser M. Acute treatment of moderate to severe depression with
hypericum extract WS 5570 (St John's wort): randomised controlled double blind non-inferiority trial
versus paroxetine. BMJ 2005;330(7490):503.
Murck H, Fava M, Alpert J, Nierenberg AA, Mischoulon D, Otto MW, Zajecka J, Mannel M,
Rosenbaum JF. Hypericum extract in patients with MDD and reversed vegetative signs: re-analysis
from data of a double-blind, randomized trial of hypericum extract, fluoxetine, and placebo. Int J
Neuropsychopharmacol 2005;8(2):215-21.
Fava M, Alpert J, Nierenberg AA, Mischoulon D, Otto MW, Zajecka J, Murck H, Rosenbaum JF.
A Double-blind, randomized trial of St John's wort, fluoxetine, and placebo in major depressive
disorder. J Clin Psychopharmacol
2005;25(5):441-7.
Simeon J, Nixon MK, Milin R, Jovanovic R, Walker S. Open-label pilot study of St. John's wort in
adolescent depression. J Child Adolesc Psychopharmacol 2005;15(2):293-301.Muller T, Mannel M,
Murck H, Rahlfs VW. Treatment of somatoform disorders with St. John's wort: a randomized, double-
blind and placebo-controlled trial. Psychosom Med 2004;66(4):538-47.
Kim HL, Streltzer J, Goebert D. St. John's wort for depression: a meta-analysis of well-defined
clinical trials. J Nerv Ment Dis 1999;187(9):532-8.
Whiskey E, Werneke U, Taylor D. A systematic review and meta-analysis of Hypericum perforatum
in depression: a comprehensive clinical review. Int Clin Psychopharmacol 2001;16(5):239-52.
Linde K, Mulrow CD, Berner M, Egger M. St John's wort for depression. Cochrane Database Syst
Rev. 2005;(2):CD000448.
Linde K, Knuppel L. Large-scale observational studies of hypericum extracts in patients with
depressive disorders-a systematic review. Phytomedicine 2005;12(1-2):148-57.
Valerio LG Jr. Review: hypericum extracts are safer and lead to fewer adverse effects than older
standard antidepressants, but have similar tolerability to SSRIs. Evid Based Ment Health
2005;8(3):71.
Grube B, Walper A, Wheatley D. St. John's Wort extract: efficacy for menopausal symptoms of
psychological origin. Adv Ther 1999;16(4):177-86.
Lawvere S, Mahoney MC, Cummings KM, Kepner JL, Hyland A, Lawrence DD, Murphy JM. A
Phase II study of St. John's Wort for smoking cessation. Complement Ther Med 2006;14(3):175-84.
Ito N., Is quercetin carcinogenetic? Jap. J Cancer Res 1992;83:313-4.
Extract from German Health Commission, BAnz 228, 05/12/84.
Millepertuis, dossier toxicologique, Travaux des Laboratoires Arkopharma, 2001.
2900.6.9.3.2 Bibliografia
Linde K, Ramirez G, Mulrow CD, Pauls A, Weidenhammer W, Melchart D. St. John's wort for
depression - an overview and meta-analysis of randomised clinical trials. Br. Med. J. 1996; 313: 253-
258.
Gaster B, Holroyd J. St. John's Wort for Depression - A Systematic Review. 2000; 160: 152-156.
Bennett DA Jr, Phun L, Polk JF, Voglino SA, Zlotnik V, Raffa RB. Neuropharmacology of St.
John's Wort (Hypericum). Ann. Pharmacother. 1998; 32: 1201-1208.
Lookmann G, Schüle C, Baghal T, Kleser M. St. John's Wort in mild to moderate depression: the
relevance of hyperforin for the clinical efficacy. Pharmacopsichiatry 1998; 31: S54-S59.
Calapai G, Crupi A, Firenzuoli F, Costantino G, Inferrera G, Campo GM, Caputi AP. Effects of
Hypericum perforatum on levels of 5-hydroxytryptamine, noradrenaline and dopamine in the cortex,
diencephalon and brainstem of the rat. J. Pharm. Pharmacol. 1999; 51: 723-728.
6 Harrer G, Schulz V. Clinical investigation of the antidepressant effectiveness of hypericum. J.
Geriatr. Psichiatry Neurol. 1994; 7 (Suppl. 1): S6-S8.
Zink T, Chaffin J. Herbal health products: what family physicians need to know. Am. Fam. Physician
1998; 58: 1133-1140.
Woelk H, Burkard G, Grunwald J. Benefits and risks of the hypericum extract LI 160: drug-
monitoring study with 3250 patients. J. Geriatr. Psichiatry Neurol. 1994; 7 (Suppl 1): S34-S38.
Schrader E, Meier B, Brattstrom A. Hypericum treatment of mild-moderate depression in a placebo-
controlled study. Hum. Psychopharmacol. 1998; 13: 163-169.
St. John's wort. Med. Lett. Drugs Ther. 1997; 39: 107-108.
Golsch S, Vocks E, Rakoski J, Brockow K, Ring J. Reversible increase in photosensitivity to UV-B
caused by St. John's wort extract. Hautarzt 1997; 48: 249-252.
Bove GM. Acue neuropathy after exposure to sun in a patient treated with St. John's wort [Letter]
Lancet 1998; 352: 1121-1122.
Brockmoller J, Reum T, Bauer S, Kerb R, Hubner WD, Roots I. Hypericin and pseudohypericin:
pharmacokinetics and effects on photosensitivity in humans. Pharmacopsichiatry 1997; 30 (Suppl. 2):
94-101.
Nierenberg AA, Burt T, Matthews J, Weiss AP. Mania associated with St. John's Wort. Biol.
Psichiatry 1999; 46: 1707-1708.
Moses EL, Mallinger AG. St. John's Wort: three cases of possible mania induction. J Clin
Psychopharmacol 2000; 20: 115-117.
Ernst E, Rand JL, Barnes J, Stevinson C. Adverse effects profile of the herbal antidepressant St.
John's wort (Hypericum perforatum L.) Eur. J. Clin. Pharmacol. 1998; 54: 589-594.
Lantz MS, Buchalter E, Giambanco V. St. John's wort and antidepressant drug interactions in the
elderly. J. Geriatr. Psichiatr. Neurol. 1999; 12: 7-10.
Demott K. St John's wort tied serotonine syndrone. Clin Psychiatry News 1998: 26; 28.
Gillman PK. Serotonin syndrome: hystory and risk. Fundam. Clin. Pharmacol. 1998; 12: 482-491.
Gordon JB. SSRIs and St John's wort: possible toxicity? Am Fam Phys. 1998: 57: 950.
Nebel A, Schneider BJ, Baker RK, Kroll DJ. Potential metabolic interaction between St John's
Worth e theophylline. Ann. Pharmacother 1999; 33: 502.
Johne A, Brockmoller J, Bauer S, Maurer A, Langheinrich M, Roots I. Pharmacokinetic
interaction of digoxin with an herbal extract from St John's wort (Hypericum perforatum). Clin
Pharmacol Ther 1999; 66: 338-345.
Fugh-Berman A. Herb-drug interactions. Lancet 2000; 355: 134-138.
Maurer A, Johne A, Bauer S, et al. Interaction of St John's wort extract with phenprocumoumon. Eur
J Clin Pharmacol 1999; 55: A22.
Ernst E. Second thoughts about safety of St John's wort. Lancet 1999; 354: 2014-2015.
2900.6.9.4 Lupolo
Delaveau P. Le Houblon. Actual Pharm 1984;(209):33-4. Verzele M. Centenary review: 100 years of hop chemistry and its
relevanceto brewing. J Inst Brew 1986;92:32-48.
De Keukeleire D, De Cooman L, Rong H, Heyerick A, Kalita J, Milligan SR.Functional properties of hop polyphenols. In:
Gross GG, Hemingway RW, Yoshida T, editors. Plant Polyphenols 2: Chemistry, Biology, Pharmacology,Ecology. New York:
Kluwer Academic/Plenum Publishers, 1999:739-60.
Wohlfart R. Humulus. In: Hänsel R, Keller K, Rimpler H, Schneider G, editors.Hagers Handbuch der pharmazeutischen
Praxis, 5th ed. Volume 5, Drogen E-O. Berlin: Springer-Verlag, 1993:447-58.
Hölzl J. Inhaltsstoffe des Hopfens (Humulus lupulus L.). Z Phytother 1992;13:155-61.
Hänsel R, Schulz J. Hopfen und Hopfenpräparate: Fragen zur pharmazeutischen Qualität. Dtsch Apoth Ztg 1986;126:2033-7.
Eri S, Khoo BK, Lech J, Hartman TG. Direct thermal desorption-gas chromatography and gas chromatography-mass
spectrometry profiling of hop (Humulus lupulus L.) essential oils in support of varietal characterization. J Agric Food Chem
2000;48:1140-9.
Sharpe FR, Laws DJR. The essential oil of hops : a review. J Inst Brew 1981;87:96-107. Hänsel R, Wohlfart R, Schmidt H.
Nachweis sedativ-hypnotischer Wirkstoffe im Hopfen. 3. Mitteilung: Der Gehalt von Hopfen und Hopfenzubereitungen an 2-
Methyl-3-buten-2-ol. Planta Med 1982;45:224-8.
Wohlfart R, Wurm G, Hänsel R, Schmidt H. Nachweis sedativ-hypnotischer Wirkstoffe im Hopfen. 5. Mitteilung: Der Abbau
der Bittersäuren zum 2- Methyl-3-buten-2-ol, einem Hopfeninhaltsstoff mit sedativ-hypnotischer
Wirkung. Arch Pharm (Weinheim) 1983;316:132-7.
McMurrough I. High-performance liquid chromatography of flavonoids in barley and hops. J Chromatogr 1981;218:683-93.
De Cooman L, Everaert E, De Keukeleire D. Quantitative analysis of hop acids, essential oils and flavonoids as a clue to the
identification of hop varieties. Phytochem Anal 1998;9:145-50.
Stevens JF, Taylor AW, Nickerson GB, Ivancic M, Henning J, Haunold A, Deinzer ML. Prenylflavonoid variation in
Humulus lupulus: distribution and taxonomic significance of xanthogalenol and 4'-O-methylxanthohumol. Phytochemistry
2000;53:759-75.
Stevens JF, Ivancic M, Hsu VL, Deinzer ML. Prenylflavonoids from Humulus lupulus. Phytochemistry 1997;44:1575-85.
Stevens JF, Taylor AW, Deinzer ML. Quantitative analysis of xanthohumol and related prenylflavonoids in hops and beer by
liquid chromatography-tandem mass spectrometry. J Chromatogr A 1999;832:97-107.
Rong H, Zhao Y, Lazou K, De Keukeleire D, Milligan SR, Sandra P. Quantitation of 8-prenylnaringenin, a novel
phytoestrogen in hops (Humulus lupulus L.), hop products and beers, by benchtop HPLC-MS using electrospray ionization.
Chromatographia 2000;51:545-52.
Milligan SR, Kalita JC, Pocock V, Van De Kauter V, Stevens JF, Deinzer ML, Rong H, De Keukeleire D. The endocrine
activities of 8-prenylnaringenin and related hop (Humulus lupulus L.) flavonoids. J Clin Endocrinol Metab 2000;85(12):4912-5.
Song-San S, Wanatabe S, Sato T. Chalcones from Humulus lupulus. Phytochemistry 1989;28:1776-8.
Fenselau C, Talalay P. Is oestrogenic activity present in hops ? Food Cosmet Toxicol 1973;11:597-603.
De Keukeleire D, Milligan SR, De Cooman L, Heyerick A. The oestrogenic activity of hops (Humulus lupulus L.) revisited.
Pharm Pharmacol Lett 1997;2/3:83-6.
Zava DT, Dollbaum CM, Blen M. Estrogen and progestin bioactivity of foods, herbs and spices. Proc Soc Exp Biol Med
1998;217:369-78.
Dixon-Shanies D, Shaikh N. Growth inhibition of human breast cancer cells by herbs and phytoestrogens. Oncol Rep
1999;6:1383-7.
(a) Milligan SR, Kalita JC, Heyerick A, Rong H, De Cooman L, De Keukeleire D. Identification of a potent phytoestrogen in
hops (Humulus lupulus L.) and beer. J Clin Endocrinol Metab 1999;63:2249-52.
(b) Milligan S, Kalita J, Pocock V, Heyerick A, De Cooman L, Rong H, De Keukeleire D. Oestrogenic activity of the hop
phyto-oestrogen, 8-prenylnaringenin. Reproduction 2002;123(2):235-42.
Kitaoka M, Kadokawa H, Sugano M, Ichikawa K, Taki M, Takaishi S et al. Prenylflavonoids: A New Class of Non-Steroidal
Phytoestrogen (Part 1). Isolation of 8-Isopentenylnaringenin and an Initial Study on its Structure-
Activity Relationship. Planta Med 1998;64:511-5.
Miranda CL, Stevens JF, Helmrich A, Henderson MC, Rodriguez RJ, Yang Y-H et al. Antiproliferative and cytotoxic effects
of prenylated flavonoids from hops (Humulus lupulus) in human cancer cell lines. Food Chem Toxicol 1999;37:271-85.
Okamoto R, Kumai A. Antigonadotropic activity of hop extract. Acta Endocrinol 1992;127:371-7.
Overk CR, Yao P, Chadwick LR, Nikolic D, Sun Y, Cuendet MA et al. Comparison of the in vitro estrogenic activities of
compounds from hops (humulus lupulus) and red clover. J Agric Food Chem 2005;53(16):6246-53.
Goetz P. Traitement des bouffées de chaleur par insuffisance ovarienne par l'extrait de houblon (Humulus lupulus). Revue de
Phytothérapie Pratique 1990;(4):13-15.
Heyerick A, Vervarcke S, Depypere H, Bracke M, De Keukeleire D. A first prospective, randomized, double-blind, placebo-
controlled study on the use of a standardized hop extract to alleviate menopausal discomforts. Maturitas 2006;54(2):164-75.
Morali G, Polatti F, Metelitsa EN, Mascarucci P, Magnani P, Marre GB. Open, non-controlled clinical studies to assess the
efficacy and safety of a medical device in form of gel topically and intravaginally used in postmenopausal
women with genital atrophy. Arzneimittelforschung 2006;56(3):230-8
Monteiro R, Becker H, Azevedo I, Calhau C. Effect of hop (Humulus lupulus L.) flavonoids on aromatase (estrogen synthase)
activity. J Agric Food Chem 2006;54(8):2938-43
Lee KM, Jung JS, Song DK, Kräuter M, Kim YH. Effects of Humulus lupulus extract on the central nervous system in mice.
Planta Med 1993;59 (Suppl):A691.
Wohlfart R, Hänsel R, Schmidt H. Nachweis sedativ-hypnotischer Wirkstoffe im Hopfen. Mitteilung : Die Pharmakologie des
Hopfeninhaltsstoffes 2-Methyl-3-buten-2-ol. Planta Med 1983;48:120-3.
Zanoli P, Rivasi M, Zavatti M, Brusiani F, Baraldi M. New insight in the neuropharmacological activity of Humulus lupulus L.
J Ethnopharmacol 2005;102(1):102-6
Piendl A, Schneider G. Uber die physiologischen Eigenschaften des Hopfens. Brauwelt 1981;121:600-8.
Schmalreck AF, Teuber M, Reininger W, Harth A. Structural features determining the antibiotic potenties of natural and
synthetic hop bitter resins, their precursors and derivatives. Can J Microbiol 1975;21:205-12.
Engelson M, Solberg M, Karmas E. Antimycotic properties of hop extract in reduced water activity media. J Food Sci
1980;45:1175-8.
Yahiro K, Shirasaka D, Tagashira M, Wada A, Morinaga N, Kuroda F, Choi O, Inoue M, Aoyama N, Ikeda M, Hirayama T,
Moss J, Noda M. Inhibitory effects of polyphenols on gastric injury by Helicobacter pylori VacA toxin. Helicobacter
2005;10(3):231-9.
Takubo M, Inoue T, Jiang S, Tsumuro T, Ueda Y, Yatsuzuka R, Segawa S, Watari J, Kamei C. Effects of hop extracts on
nasal rubbing and sneezing in BALB/c mice. Biol Pharm Bull 2006;29(4):689-92.
Yasukawa K, Yamaguchi A, Arita J, Sakurai S, Ikeda A, Takido M. Inhibitory effect of edible plant extracts on 12-O-
tetradecanoylphorbol-13-acetate-induced ear oedema in mice. Phytother Res 1993;7:185-9.
Yasukawa K, Takeuchi M, Takido M. Humulon, a bitter in the hop, inhibits humor promotion by 12-O-tetradecanoylphorbol-
13-acetate in two-stage carcinogenesis in mouse skin. Oncology (Basel) 1995:52:156-8.
Zhao F, Nozawa H, Daikonnya A, Kondo K, Kitanaka S. Inhibitors of nitric oxide production from hops (Humulus lupulus L.).
Biol Pharm Bull 2003;26(1):61-5.
Bohr G, Gerhauser C, Knauft J, Zapp J, Becker H. Anti-inflammatory acylphloroglucinol derivatives from Hops (Humulus
lupulus). J Nat Prod 2005;68(10):1545-8.
Hougee S, Faber J, Sanders A, Berg WB, Garssen J, Smit HF, Hoijer MA. Selective inhibition of COX-2 by a standardized
CO2 extract of Humulus lupulus in vitro and its activity in a mouse model of zymosan-induced arthritis. Planta Med
2006;72(3):228-33.
Delmulle L, Bellahcene A, Dhooge W, Comhaire F, Roelens F, Huvaere K, Heyerick A, Castronovo V, De Keukeleire D.
Anti-proliferative properties of prenylated flavonoids from hops (Humulus lupulus L.) in human prostate cancer cell lines.
Phytomedicine 2006;13(9-10):732-4.
Gerhauser C, Alt A, Heiss E, Gamal-Eldeen A, Klimo K, Knauft J, Neumann I, Scherf HR, Frank N, Bartsch H, Becker H.
Cancer chemopreventive activity of Xanthohumol, a natural product derived from hop. Mol Cancer Ther 2002;1(11):959-69.
Colgate EC, Miranda CL, Stevens JF, Bray TM, Ho E. Xanthohumol, a prenylflavonoid derived from hops induces apoptosis
and inhibits NF-kappaB activation in prostate epithelial cells. Cancer Lett. 2007;246(1-2):201-9.
Dietz BM, Kang YH, Liu G, Eggler AL, Yao P, Chadwick LR, Pauli GF, Farnsworth NR, Mesecar AD, van Breemen RB,
Bolton JL. Xanthohumol isolated from Humulus lupulus Inhibits menadione-induced DNA damage through induction of quinone
reductase. Chem Res Toxicol 2005;18(8):1296-305.
Pan L, Becker H, Gerhauser C. Xanthohumol induces apoptosis in cultured 40-16 human colon cancer cells by activation of
the death receptor- and mitochondrial pathway. Mol Nutr Food Res 2005;49(9):837-43.
Chen WJ, Lin JK. Mechanisms of cancer chemoprevention by hop bitter acids (beer aroma) through induction of apoptosis
mediated by Fas and caspase cascades. J Agric Food Chem 2004;52(1):55-64.
Nozawa H. Xanthohumol, the chalcone from beer hops (Humulus lupulus L.), is the ligand for farnesoid X receptor and
ameliorates lipid and glucose metabolism in KK-A(y) mice. Biochem Biophys Res Commun 2005;336(3):754-61.
Yajima H, Ikeshima E, Shiraki M, Kanaya T, Fujiwara D, Odai H, Tsuboyama- Kasaoka N, Ezaki O, Oikawa S, Kondo K.
Isohumulones, bitter acids derived from hops, activate both peroxisome proliferator-activated receptor alpha and gamma and
reduce insulin resistance. J Biol Chem 2004;279(32):33456-62.
Buckwold VE, Wilson RJ, Nalca A, Beer BB, Voss TG, Turpin JA, Buckheit RW 3rd, Wei J, Wenzel-Mathers M, Walton
EM, Smith RJ, Pallansch M, Ward P, Wells J, Chuvala L, Sloane S, Paulman R, Russell J, Hartman T, Ptak R. Antiviral
activity of hop constituents against a series of DNA and RNA viruses. Antiviral Res 2004;61(1):57-62.
Schilcher H. Pflanzliche Psychopharmaka. Eine neue Klassifizierung nach Indikationsgruppen. Dtsch Apoth Ztg
1995;135:1811-22.
Hänsel R. Pflanzliche Beruhigungsmittel. Möglichkeiten und Grenzen in der Selbstmedikation. Dtsch Apoth Ztg
1995;135:2935-43. Wichtl M. Lupuli strobulus - Hopfenzapfen. In: Wichtl M, editor. Teedrogen, 3rd ed. Stuttgart:
Wissenschaftliche Verlagsgesellschaft, 1997:356-9. - Humulus. In: British Herbal Pharmacopoeia 1983. Bournemouth: British
Herbal Medicine Association, 1983:111-2.
Schilcher H. Sedatives. In: Phytotherapy in Paediatrics. Handbook for Physicians and Pharmacists (translation of
Phytotherapie in der Kinderheilkunde, 2nd ed.). Stuttgart: Medpharm Scientific, 1997:58-62.
Houblon, dossier toxicologique. Travaux des Laboratoires ARKOPHARMA.
2900.6.9.5 Melissa
Sanders RW, Cantino PD. Nomenclature of the subdivisions of the Lamiaceae. Taxon 1984;33:64-72.
Koch-Heitzmann I, Schultze W. (a) - Melissa officinalis L. Eine alte Arzneipflanze mit neuen therapeutischen Wirkungen.
Dtsch Apoth Ztg 1984;124:2137-45. (b) - 2000 Jahre Melissa officinalis. Von der Bienenpflanze zum Virustatikum. Z Phytother
1988;9:77-85. voir aussi : Mulkens A. Etude phytochimique des feuilles de Melissa officinalis L. (Lamiaceae). Thèse de Doct.
ès Sciences, Sciences Pharmaceutiques, Univ. de Genève, n° 2255, 1987.
Mulkens A, Kapetanidis I. Flavonoïdes des feuilles de Melissa officinalis L. (Lamiaceae). Pharm Acta Helv 1987;62:19-22.
Gracza L, Ruff P. Über Vorkommen und Analytik von Phenylpropanderivaten. 5. Mitt. : Rosmarinsäure in Arzneibuchdrogen
und ihre HPLC-Bestimmung. Arch Pharm (Weinheim) 1984;317:339-45.
Tittel G, Wagner H, Bos R. Über die chemische Zusammensetzung von Melisssenölen. Planta Med 1982;46:91-8.
(a) - Mulkens A, Kapetanidis I. Etude de l'huile essentielle de Melissa officinalis L. (Lamiaceae). Pharm Acta Helv
1988;63:266-70.
(b) - Dawson BSW, Franich RA, Meder R. Essential oil of Melissa officinalis L. subsp. Altissima (Sibthr. et Smith) Arcang.
Flavour and Fragrance J 1988;3:167-70.
(c) – Schultze W. Die Melisse. Dünnschichtchromatographische Untersuchung des ätherischen Öles. Dtsch Apoth Ztg
1989;129:155-63.
Patora J, Majda T, Gora J, Klimek B. Variability in the content and composition of essential oil from lemon balm (Melissa
officinalis L.) cultivated in Poland. Acta Pol Pharm 2003;60(5):395-400.
Enjalbert F, Bessiere JM, Pellecuer J, Privat G. Analyse des essences de mélisse. Fitoterapia 1983;54:59-65.
Mulkens A, Kapetanidis I. Hétérosides à génines volatiles dans les feuilles de Melissa officinalis L. (Lamiaceae). Pharm Acta
Helv 1985;60:276-8.
Mimica-Dukic N, Bozin B, Sokovic M, Simin N. Antimicrobial and antioxidant activities of Melissa officinalis L. (Lamiaceae)
essential oil. J Agric Food Chem 2004;52(9):2485-9.
Dikshit A, Husain A. Antifungal action of some essential oils against animal pathogens. Fitoterapia 1984;55:171-6.
De Sousa AC, Alviano DS, Blank AF, Alves PB, Alviano CS, Gattass CR. Melissa officinalis L. essential oil: antitumoral and
antioxidant activities. J Pharm Pharmacol 2004;56(5):677-81.
Ferreira A, Proenca C, Serralheiro ML, Araujo ME. The in vitro screening for acetylcholinesterase inhibition and antioxidant
activity of medicinal plants from Portugal. J Ethnopharmacol 2006;108(1):31-7.
Marongiu B, Porcedda S, Piras A, Rosa A, Deiana M, Dessi MA. Antioxidant activity of supercritical extract of Melissa
officinalis subsp. officinalis and Melissa officinalis subsp. inodora. Phytother Res 2004;18(10):789-92.
Allahverdiyev A, Duran N, Ozguven M, Koltas S. Antiviral activity of the volatile oils of Melissa officinalis L. against Herpes
simplex virus type-2. Phytomedicine 2004;11(7-8):657-61.
Wölbling RH, Milbradt R. Klinik und Therapie des Herpes simplex – Vorstellung eines neuen phytotherapeutischen
Wirkstoffes. Therapiewoche 1984;34:1193-1200.
Chlabicz J, Galasinski W. The components of Melissa officinalis L. that influence protein biosynthesis in-vitro. J Pharm
Pharmacol 1986;38:791-4.
(a) - Sticher O. Plant mono-, di-, and sesquiterpenoids with pharmacological or therapeutical activity. In : New natural products
and plant drugs with pharmacological, biological or therapeutical activity. Wagner H, Wolff P éds. Springer-Verlag. 1977:137-
76.
(b) - Reiter M, Brandt W. Relaxant effects on tracheal and ileal smooth muscles of the guinea pig. Arzneimittelforschung
1985;35:408-14.
Sadraei H, Ghannadi A, Malekshahi K. Relaxant effect of essential oil of Melissa officinalis and citral on rat ileum
contractions. Fitoterapia 2003;74(5):445-52.
Sourgens H, Winterhoff H, Gumbiger HG, Kemper FH. Antihormonal effects of plant extracts. TSH and prolactin-
suppressing properties of Lithospermum officinale and other plants. Planta Med 1982;45:78-86.
Auf'mkolk M, Amir SM, Kubota K, Ingbar SH. The active principles of plant extracts with antithyrotropic activity : oxidation
products of derivatives of 3,4- dihydroxycinnamic acid. Endocrinology 1985;116:1677-86.
Drozd J, Anuszewska E. The effect of the Melissa officinalis extract on immune response in mice. Acta Pol Pharm
2003;60(6):467-70
Bolkent S, Yanardag R, Karabulut-Bulan O, Yesilyaprak B. Protective role of Melissa officinalis L. extract on liver of
hyperlipidemic rats: a morphological and biochemical study. J Ethnopharmacol 2005;99(3):391-8.
Dudai N, Weinstein Y, Krup M, Rabinski T, Ofir R. Citral is a new inducer of caspase-3 in tumor cell lines. Planta Med
2005;71(5):484-8.
Büchner KH, Hellings H, Huber M, Peukert E, Späth L, Deininger R. Doppelblindstudie zum Nachweis der therapeutischen
Wirkung von Melissengeist bei psychovegetativen Syndromen. Med Klin 1974;69:1032-6.
Dressing H, Riemann D, et al. Insomnia: Are valerian/balm combinations of equal value to benzodiazepine ? (translated from
German) Therapiewoche 1992;42:726–736.
Cerny A, Schmid K. Tolerability and efficacy of valerian/lemon balm in healthy volunteers (a double-blind, placebo-controlled,
multicentre study). Fitoterapia 1999;70:221–228.
Muller SF, Klement S. A combination of valerian and lemon balm is effective in the treatment of restlessness and dyssomnia
in children. Phytomedicine 2006;13(6):383-7.
Savino F, Cresi F, Castagno E, Silvestro L, Oggero R. A randomized doubleblind placebo-controlled trial of a standardized
extract of Matricariae recutita, Foeniculum vulgare and Melissa officinalis (ColiMil) in the treatment of breastfed colicky infants.
Phytother Res 2005;19(4):335-40.
Kennedy DO, Little W, Scholey AB. Attenuation of laboratory-induced stress in humans after acute administration of Melissa
officinalis (Lemon Balm).Psychosom Med 2004;66(4):607-13.
Kennedy DO, Scholey AB, et al. Modulation of mood and cognitive performance following acute administration of Melissa
officinalis (lemon balm). Pharmacol Biochem Behav 2002;72(4):953-64.
Ballard CG, O'Brien JT, Reichelt K, Perry EK. Aromatherapy as a safe and effective treatment for the management of
agitation in severe dementia: the results of a double-blind, placebo-controlled trial with Melissa. J Clin
Psychiatry 2002;63(7):553-8 ; voir commentaire In: J Clin Psychiatry 2003;64(6):732 et la réponse de l'auteur.
2900.6.9.6 Passiflora
2900.6.9.6.1 Scientifico
Brasseur T., Angenot L. Contribution à l'étude pharmacognostique de la Passiflore. J Pharm Belg 1984;39:15-22.
Dhawan K, Kumar S, Sharma A. Comparative biological activity study on Passiflora incarnata and P. edulis. Fitoterapia
2001;72(6):698-702.
Wagner H, Tittel G, Bladt S. Analyse und standardisierung von Arzneidrogen und Phytopräparaten durch
Hochleistungsflüssigchromatographie (HPLC) und andere chromatographische Verfahren. Dtsch Apoth Ztg 1983;123:515-21.
Pietta P, Manera E, Ceva P. Isocratic liquid chromatographic method for the simultaneous determination of Passiflora
incarnata L. and Crataegus monogyna flavonoids in drugs. J Chromatogr 1986;(357):233-8.
Olafsdottir ES, Andersen JV, Jaroszewski J. Cyanohydrin glycosides of Passifloraceae. Phytochemistry 1989;28:127-
32; voir aussi : Spencer KC, Seigler DS. Gynocardin from Passiflora. Planta Med 1984;50:356-7.
Lutomski J, Segiet E, Szpunar K, Grisse K. Die Bedeutung der Passionsblüme in der Heilkunde. Pharm Unserer Zeit
1981;10:45-9.
Congora C, Proliac A, Raynaud J. Isolement et identification de deux glucosyl- lutéolines mono-C-substituées et de la
diglucosyl-6,8-lutéoline di-C substituée dans les tiges feuillées de Passiflora incarnata. Helv Chim Acta 1986;69:251-3.
Geiger H, Markham KR. The C-glycosylflavone pattern of Passiflora incarnata L. Z Naturforsch 1986;41c:949-50.
Proliac A, Raynaud J. O-glucosyl-2''-C-glucosyl-6 apigénine de Passiflora incarnata L. (Passifloraceae). Pharm Acta Helv
1988;63:174-5.
Aoyagi N, Kimura R, Murata T. Studies on Passiflora incarnata dry extract : I. Isolation of maltol and pharmacological
action of maltol and ethylmaltol. Chem Pharm Bull (Tokyo) 1974;22:1008-13.
Speroni E, Minghetti A. Neuropharmacological activity of extracts from Passiflora incarnata. Planta Med 1988;54:488-91.
Sopranzi N, De Feo G, Mazzanti G, Tolu L. Parametri biologici ed elettroencefalografici nel ratto correlati a Passiflora
incarnata L. Clin Ter 1990;132:329-33.
Galliano G, Foussard-Blanpin O, Bretaudeau J. Etude expérimentale du rôle du maltol dans les propriétés psycho-
pharmacologiques de Passiflora incarnata L. (Passifloracées). Phytotherapy 1994;(40/41):18-22.
Speroni E, Billi R, Mercati V, Boncompagni E, Toja E. Sedative effects of crude extract of Passiflora incarnata after
oral administration. Phytother Res 1996;10:S92-4.
15. Passiflore, dossier toxicologique. Travaux des Laboratoires ARKOPHARMA.
Soulimani R, Younos C, Jarmouni S, Bousta D, Misslin R, Mortier F. Behavioural effects of Passiflora incarnata L.
and its indole alkaloid and flavonoids derivatives and maltol in the mouse. J Ethnopharmacol 1997;57(1):11-20.
Müller WE, Fehske KJ, Borbe HO, Wollert U, Nanz C, Rommelspacher H. On the neuropharmacology of harmane
and other b-carbolines. Pharmacol Biochem Behav 1981;14:693-9; voir aussi : Bidet D. et al. Actual Chim 1984:17-30;
Rommelspacher H. et al. Eur J Pharmacol 1981;70:409-16; Pierard
C. Les b-carbolines d'origine naturelle et leur intérêt biologique. Thèse de Dr. Pharm. (D.E.) Paris V. 1984.
Dhawan K, Kumar S, Sharma A. Anti-anxiety studies on extracts of Passiflora incarnata Linneaus. J Ethnopharmacol
2001;78(2-3):165-70.
Dhawan K, Kumar S, Sharma A. Suppression of alcohol-cessation-oriented hyper-anxiety by the benzoflavone moiety of
Passiflora incarnata Linneaus in mice. J Ethnopharmacol 2002;81(2):239-44.
Dhawan K, Kumar S, Sharma A. Reversal of cannabinoids (delta9-THC) by the benzoflavone moiety from methanol
extract of Passiflora incarnata Linneaus in mice: a possible therapy for cannabinoid addiction. J Pharm Pharmacol
2002;54(6):875-81.
Dhawan K, Dhawan S, Chhabra S. Attenuation of benzodiazepine dependence in mice by a tri-substituted benzoflavone
moiety of Passiflora incarnate Linneaus: a non-habit forming anxiolytic. J Pharm Pharm Sci 2003;6(2):215-22.
Dhawan K, Sharma A. Prevention of chronic alcohol and nicotine-induced azospermia, sterility and decreased libido, by a
novel tri-substituted benzoflavone moiety from Passiflora incarnata Linneaus in healthy male rats. Life Sci 2002;71(26):3059-
69.
Dhawan K, Kumar S, Sharma A. Aphrodisiac activity of methanol extract of leaves of Passiflora incarnata Linn in mice.
Phytother Res 2003;17(4):401-3.
Dhawan K, Sharma A. Antitussive activity of the methanol extract of Passiflora incarnata leaves. Fitoterapia
2002;73(5):397-9.
Dhawan K, Kumar S, Sharma A. Antiasthmatic activity of the methanol extract of leaves of Passiflora incarnata. Phytother
Res 2003;17(7):821-2.
Oga S, de Freitas PCD, Gomes da Silva AC, Hanada S. Pharmacological trials of crude extract of Passiflora alata. Planta
Med 1984;50:303-6. Sur P. alata voir : Ulubelen A. et al. J Nat Prod 1982;45:783.
Cavazzuti GB. Etude pharmacologique clinique d'une association de GABOB et d'extraits végétaux utilisée chez l'enfant
ayant des troubles du comportement et du sommeil. Clin Ter 1969;51:15-29.
Delaveau P. La passiflore. Actual Pharm 1985;(227).
Akhondzadeh S, Naghavi HR, Vazirian M, Shayeganpour A, Rashidi H, Khani M. Passionflower in the treatment of
generalized anxiety: a pilot doubleblind randomized controlled trial with oxazepam. J Clin Pharm Ther 2001;26(5):363-7.
Akhondzadeh S, Kashani L, Mobaseri M, Hosseini SH, Nikzad S, Khani M. Passionflower in the treatment of opiates
withdrawal: a double-blind randomized controlled trial. J Clin Pharm Ther 2001;26(5):369-73.
(a) - Ross MSF, Anderson LA. Selection of plants for phytopharmacological study based on modern herbal practice. Int J
Crude Drug Res 1986;24:1-6. (b) - Bizet D, Roubaudi F. La passiflore, Passiflora incarnata L. Passifloracées. Phytotherapy
1988;26:22-4.
2900.6.9.6.2 Fitovigilanza
1 Newall, C.A., Anderson LA, Phillipson JD. 1996. Herbal Medicines: A Guide for Health-Care
Professionals. London: The Pharmaceutical Press.
2 Bradley, P.R. (ed.). 1992. British Herbal Compendium, Vol. 1. Bournemouth: British Herbal
Medicine Association.
3 Gerhard U, Hobi V, Kocher R, Konig C. Acute sedative effect of a herbal relaxation tablet as
compared to that of bromazepam. Schweiz Rundsch Med. Prax 1991; 80: 1481-1486.
4 Bruneton, J. 1995. Pharmacognosy, Phytochemistry, Medicinal Plants. Paris: Lavoisier Publishing.
5 AoyagiN, Kimura R, Murata T,. Studies on Passiflora incarnata dry extract . I. Isolation of maltol
and pharmacological action of maltol and ethyl maltol. Chem Pharm Bull 1974; 22: 1008-1013.
6 Brasseur T, Angenot L. The Pharmacognosy of the passion flower. J. Pharm. Belg. 1984; 39: 15-
22.
7 Li QM, van de Heuvel H, Delorenzo O, Corthout J, Pieters LA, Vlietnick AJ, Claeys M. Mass
spectral characterization of C-glycosidic flavonoids isolated from a medicinal plant (Passiflora
incarnata). J. Chromatogr. 1991; 562: 435-446.
8 Rehwald A, Meier B, Stcher O. Qualitative and quantitative reversed-phase high-performance
liquid chromatography of flavonoids in Passiflora incarnata L. Pharm. Acta Helv. 1994; 69: 153-158.
9 ESCOP. 1997. "Passiflorae herba." Monographs on the Medicinal Uses of Plant Drugs. Exeter,
U.K.: European Scientific Cooperative on Phytotherapy.
10 Bisset NG. Passiflorae herba. In: Herbal drugs and phytopharmaceuticals: a handbook for
practice on a scientific basis. Stuttgart: medpharm, Boca raton-London: CRC Press, 1994; 363-365.
11 Smith GW, Chalmers TM, Nuki G. Vasculitis associated with herbal preparation containing
Passiflora extract. Br. J. Rheumatol. 1993; 32: 87-88.
12 Solbakken AM, Rorbakken G, Gundersen T. Nature medicine as intoxicant. Tidsskr Nor
Laegeforen 1997; 117: 1140-1141.
13 Giavina-Bianchi PF Jr, Castro FF, Machado ML, Duarte AJ. Occupational respiratory allergic
disease induced by Passiflora alata and Rhamnus purshiana. Ann. Allergy Asthma Immunol. 1997;
79: 449-454.
14 Fisher AA, Purcell P, Le Couter DG. Toxicity of Passiflora incarnata L. Clinical Toxicology 2000;
38: 63-66.
2900.6.9.7 Rodiola
2900.6.9.7.1 Fitovigilanza
-1- Ming DS, et al. Bioactive compounds from Rhodiola rosea (Crassulaceae). Phytother Res 2005;
19: 740–743.
-2- Spasov AA, et al. A double-blind, placebo-controlled pilot study of the stimulating and
adaptogenic effect of Rhodiola rosea SHR-5 extract on the fatigue of students caused by stress
during an examination period with a repeated low-dose regimen. Phytomedicine 2000; 7: 85–89.
-3- Mattioli L, Perfumi M. Rhodiola rosea L. extract reduces stress- and CRF-induced anorexia in
rats. J Psychopharmacol 2007; 21: 742–750.
-4- Brown RP, et al. Rhodiola rosea. A phytochemical overview. Herbalgram 2002; 56: 40–52.
-5- Kucinskaite A, et al. Evaluation of biologically active compounds in roots and rhizomes of
Rhodiola rosea L. cultivated in Lithuania. Medicina (Kaunas) 2007; 43: 487–494.
-6- Hellum BH, et al. Potent in vitro inhibition of CYP3A4 and P-glycoprotein by Rhodiola rosea.
Planta Med 2010; 76: 331-8.
2900.6.9.8 Valeriana
2900.6.9.8.1 Biblio
generale
Freytag WE. Bestimmung von Valerensäuren und Valerenal neben Valepotriaten in Valeriana
officinalis durch HPLC. Pharmazeutische Ztg. 1983;128:2869-71; voir aussi : Hänsel R et al. Pharm
Ind 1985;47:531-3.
Houghton PJ. The biological activity of valerian and related plants. J Ethnopharmacol 1988;22:121-
42.
Janot MM, Guilhem J, Contz O, Georgescu V, Cionga E. Contribution à l'étude des alcaloïdes de
la valériane (Valeriana officinalis) actinidine et naphtyridylméthylcétone : nouvel alcaloïde. Ann Pharm
Fr 1979;37:413-20.
Urban JD. Etudes chimiques et pharmacologiques préliminaires de nouvelles formes galéniques de
Valériane, Valeriana officinalis (L.) D.C., Thèse de Doctorat en Pharmacie, Strasbourg, 1987.
Bos R, Hendricks H, Bruins AP, Klosterman J, Sipma G. Isolation and identification of valerenane
sesquiterpenoids from Valeriana officinalis. Phytochemistry 1986;25:133-5.
Mikhova BP, Handjeva NV, Popov SS, Passov SL. Structural investigation of valepotriates on the
basis of 1H-lanthanide-induced shifts. J Nat Prod 1987;50:1141-5.
Marekov Nl, Popov SS, Handjieva NV. Chemistry of pharmaceutically important cyclopentane
monoterpenes from some Valeriana plants. In : Chemistry and Biotechnology of Biologically Active
Natural Products. 2nd Int. Conf. Budapest 1983. Szantay CS, Gottsegen A, Kovacs G. éds.
Amsterdam. Elsevier 1984:313-29.
Wagner H, Jurcic K, Schaette R. Vergleichende Untersuchungen über die sedierende Wirkung von
Baldrianextrakten, Valepotriaten und ihren Abbauprodukten. Planta Med 1980;38:358-65.
Ammelounx P, Holm E, Langhans W, Scherer HD, Blatter J. Vergleichende neurophysiologische
Untersuchungen mit Valepotriaten und Extraktum Valerianae an Katzen. Planta Med 1978;33:282-3.
Bounthanh C. Etude de quelques propriétés pharmacologiques des valépotriates, molécules isolées
des racines de Valerina wallichii (L.) D.C., Thèse de Doctorat ès Sciences, Strasbourg, 1985.
Hendricks H, Bos R, Woerdenbag HJ, Koster ASj. Central nervous depressant activity of valerenic
acid in the mouse. Planta Med 1985;51:28-31; voir aussi : Hendricks H et al. ibid. 1981;42:62-8.
Riedel E, Hänsel R, Ehrke G. Hemmung des g-Aminobuttersäureabbaus durch
Valerensäurederivate. Planta Med 1982;46:219-20.
Santos MS, Ferreira F, Cunha AP, Carvalho AP, Ribeiro CF, Macedo T. Synaptosomal GABA
release as influenced by valerian root extract—involvement of the GABA carrier. Arch Int
Pharmacodyn Ther 1994;327(2):220-31.
Ortiz JG, Nieves-Natal J, Chavez P. Effects of Valeriana officinalis extracts on [3H]flunitrazepam
binding, synaptosomal [3H]GABA uptake, and hippocampal [3H]GABA release. Neurochem Res
1999;24(11):1373-8.
De Feo V, Faro C. Pharmacological effects of extracts from Valeriana adscendens Trel. II. Effects on
GABA uptake and amino acids. Phytother Res 2003;17(6):661-4.
Yuan CS, Mehendale S, Xiao Y, Aung HH, Xie JT, Ang-Lee MK. The gammaaminobutyric acidergic
effects of valerian and valerenic acid on rat brainstem neuronal activity. Anesth Analg
2004;98(2):353-8.
Dietz BM, Mahady GB, Pauli GF, Farnsworth NR. Valerian extract and valerenic acid are partial
agonists of the 5-HT5a receptor in vitro. Brain Res Mol Brain Res 2005;138(2):191-7.
Muller CE, Schumacher B, Brattstrom A, Abourashed EA, Koetter U. Interactions of valerian
extracts and a fixed valerian-hop extract combination with adenosine receptors. Life Sci
2002;71(16):1939-49.
Fernandez S, Wasowski C, Paladini AC, Marder M. Sedative and sleepenhancing properties of
linarin, a flavonoid-isolated from Valeriana officinalis. Pharmacol Biochem Behav 2004;77(2):399-404.
Marder M, Viola H, Wasowski C, Fernandez S, Medina JH, Paladini AC. 6- methylapigenin and
hesperidin: new valeriana flavonoids with activity on the CNS. Pharmacol Biochem Behav
2003;75(3):537-45.
Shinomiya K, Fujimura K, Kim Y, Kamei C. Effects of valerian extract on the sleep-wake cycle in
sleep-disturbed rats. Acta Med Okayama 2005;59(3):89-92.
Wagner H, Jurcic K. On the spasmolytic activity of Valeriana extracts. Planta Med1979;37:84-95.
Hazelhoff B, Malingre TM, Meijer DKF. Antispasmodic effects of Valeriana compounds : an in vivo
and in vitro study on the Guinea-Pig ileum. Arch int Pharmacodyn 1982;257:274-7.
Gilani AH, Khan AU, Jabeen Q, Subhan F, Ghafar R. Antispasmodic and blood pressure lowering
effects of Valeriana wallichii are mediated through K+ channel activation. J Ethnopharmacol
2005;100(3):347-52.
Anton R, Haag M, Kuballa B. Biological and therapeutic activity. The evaluation of substances
derived from natural sources. In : Advances in medicinal phytochemistry. Barton D, Ollis WD, éds.
Londres. John Libbey. 1986:13-23.
Von der Hude W, Scheutwinkel-Reich M, Braun R. Bacterial mutagenicity of the tranquilizing
constituents of Valerianaceae roots. Mutation Res 1986;169:23-7; voir aussi, sur l'activité des
baldrinals : Braun R et al. Planta Med 1986;52:446-50.
Si XY, Jia RH, Huang CX, Ding GH, Liu HY. Effects of Valeriana officinalis var. latifolia on
expression of transforming growth factor beta 1 in hypercholesterolemic rats. Zhongguo Zhong Yao
Za Zhi 2003;28(9):845-8.
Malva JO, Santos S, Macedo T. Neuroprotective properties of Valeriana officinalis extracts.
Neurotox Res 2004;6(2):131-40.
Andreatini R, Sartori VA, Seabra ML, Leite JR. Effect of valepotriates (valerian extract) in
generalized anxiety disorder: a randomized placebo-controlled pilot study. Phytother Res
2002;16(7):650-4.
Donath F, Quispe S, Diefenbach K, Maurer A, Fietze I, Roots I. Critical evaluation of the effect of
valerian extract on sleep structure and sleep quality. Pharmacopsychiatry 2000;33(2):47-53.
Dorn M. Efficacy and tolerability of Baldrian versus oxazepam in non-organic and non-psychiatric
insomniacs: a randomised, double-blind, clinical, comparative study. Forsch Komplementarmed Klass
Naturheilkd 2000;7(2):79-84.
Ziegler G, Ploch M, Miettinen-Baumann A, Collet W. Efficacy and tolerability of valerian extract LI
156 compared with oxazepam in the treatment of non-organic insomnia—a randomized, double-blind,
comparative clinical study. Eur J Med Res 2002;7(11):480-6.
Herrera-Arellano A, Luna-Villegas G, Cuevas-Uriostegui ML, Alvarez L, Vargas-Pineda G,
Zamilpa-Alvarez A, Tortoriello J. Polysomnographic evaluation of the hypnotic effect of Valeriana
edulis standardized extract in patients suffering from insomnia. Planta Med 2001;67(8):695-9.
Dominguez RA, Bravo-Valverde RL, Kaplowitz BR, Cott JM. Valerian as a hypnotic for Hispanic
patients. Cultur Divers Ethnic Minor Psychol 2000;6(1):84-92.
Cropley M, Cave Z, Ellis J, Middleton RW. Effect of kava and valerian on human physiological and
psychological responses to mental stress assessed under laboratory conditions. Phytother Res
2002;16(1):23-7.
Francis AJ, Dempster RJ. Effect of valerian, Valeriana edulis, on sleep difficulties in children with
intellectual deficits: randomised trial. Phytomedicine 2002;9(4):273-9.
Leathwood PD, Chauffard F. Aqueous extract of valerian reduces latency to fall asleep in Man.
Planta Med. 1985;51:144-8.
Leathwood PD, Chauffard F. Quantifying the effects of mild sedatives. J Psychiatr Res 1983;17:115-
22;
Leathwood PD et al. Pharmacol Biochem Behav 1982;17:65-71.
Fussel A, Wolf A, Brattstrom A Effect of a fixed valerian-Hop extract combination (Ze 91019) on
sleep polygraphy in patients with non-organic insomnia: a pilot study. Eur J Med Res 2000;5(9):385-
90.
(a) Wheatley D. Kava and valerian in the treatment of stress-induced insomnia. Phytother Res
2001;15(6):549-51.
(b) Wheatley D. Stress-induced insomnia treated with kava and valerian: singly and in combination.
Hum Psychopharmacol 2001;16(4):353-6.
Kennedy DO, Little W, Haskell CF, Scholey AB. Anxiolytic effects of a combination of Melissa
officinalis and Valeriana officinalis during laboratory induced stress. Phytother Res 2006;20(2):96-
102.
Muller SF, Klement S. A combination of valerian and lemon balm is effective in the treatment of
restlessness and dyssomnia in children. Phytomedicine 2006;13(6):383-7.
Muller D, Pfeil T, von den Driesch V. Treating depression comorbid with anxiety—results of an open,
practice-oriented study with St John's wort WS 5572 and valerian extract in high doses.
Phytomedicine 2003;10 Suppl 4:25-30.
Yang GY, Wang W. Clinical studies on the treatment of coronary heart disease with Valeriana
officinalis var latifolia. Zhongguo Zhong Xi Yi Jie He Za Zhi 1994;14(9):540-2.
Valériane, dossier toxicologique. Travaux des Laboratoires ARKOPHARMA.
Ugalde M, Reza V, Gonzalez-Trujano ME, Avula B, Khan IA, Navarrete A. Isobolographic analysis
of the sedative interaction between six central nervous system depressant drugs and Valeriana edulis
hydroalcoholic extract in mice. J Pharm Pharmacol 2005;57(5):631-9.
Gurley BJ, Gardner SF, Hubbard MA, Williams DK, Gentry WB, Khan IA, Shah A. In vivo effects
of goldenseal, kava kava, black cohosh, and valerian on human cytochrome P450 1A2, 2D6, 2E1,
and 3A4/5 phenotypes. Clin Pharmacol Ther 2005;77(5):415-26.
Donovan JL, DeVane CL, Chavin KD, Wang JS, Gibson BB, Gefroh HA, Markowitz JS. Multiple
night-time doses of valerian (Valeriana officinalis) had minimal effects on CYP3A4 activity and no
effect on CYP2D6 activity in healthy volunteers. Drug Metab Dispos 2004;32(12):1333-6.
2900.6.9.8.2 Biblio
1 European Medicines Agency (EMEA) – Evaluation of Medicines for Human Use. Community herbal Monograph on Valerian root (Valeriana, radix). Doc. Ref. EMEA/HMPC/340719/2005, 2005; 1-5. 2 PDR for Herbal Medicines – Third Edition, Thomson PDR at Montvale, U.S.A, 2004;852-856.
3 Bent S, Padula A, Moore D, Patterson M, Mehling W. Valerian for sleep: a systematic review
and meta-analysis. Am. J. Med. 2006; 119, 1005-1012.
4 Shimazaki M, Martin JL. Do herbal agents have a place in the treatment of sleep problems in
long-term care? J. Am. Med. Dir. Assoc. 2007; 8: 248-252.
5 Cupp MJ. Toxicology and clinical pharmacology of herbal products, Humana Press, New Jersey,
2000; 53-66.
6 Hadley S, Petry JJ. Valerian. Am. Farm. Physician 2003;67: 1755-1758.
7 Capasso F, Grandolini G, Izzo, AA. Fitoterapia – Impiego razionale delle droghe vegetali,
Springer, Italia, 2006; 242-3.
8 Houghton PJ. The scientific basis for the reputed activity of valerian. J. Pharm. Pharmacol. 1999;
51: 505-512.
9 Poyares DR , Guilleminault C, Ohayon MM, Tufik S. Can valerian improve the sleep of
insomniacs after benzodiazepine withdrawal? Prog. Neuropsychopharmacol. Biol. Psychiatry. 2002;
26(3): 539-545.
10 Donath F, Quispe S, Diefenbach K, Maurer A, Fietze I, Roots I. Critical evaluation of the effect
of valerian extract on sleep srtucture and sleep quality. Pharmacopsyhiatry 2000; 33: 47-53.
11 Taibi DM, Landis CA, Petry H, Vitiello MV. A systematic review of valerian as a sleep aid: Safe
but not effective. Sleep Med Rev. 2007; 11(3): 209-230.
12 Miyasaka LS, Atallah AN, Soares BG. Valerian for anxiety disorders. Cochrane Database Syst
Rev 2006; 4: CD004515.
13 Hazelhoff B, Malingre TM, Meijer DK. Antispasmodic effects of valeriana compounds: an in-
vivo and in-vitro study on the guinea-pig ileum. Arch. Int. Pharmacodyn. Ther. 1982; 257: 274-287.
14 Leuschner J, Muller J, Rudmann M. Characterisation of the central nervous depressant activity
of a commercially available valerian root extract. Arzneimittelforschung 1993; 43: 638-641.
15 National Standard Research Collaboration. Valerian (Valeriana officinalis L.).
www.nlm.nih.gov/medlineplus/druginfo/natural/patient-valerian.htlm 2006.
16 Jacobo-Herrera NJ, Vartiainen N, Bremner P, Gibbons S, Koistinaho J, Heinrich M. NF-
kappaB modulators from Valeriana officinalis. Phytother. Res. 2006; 20(10): 917-919.
17 Circosta C, De Pasquale R, Samperi S, Pino A, Occhiuto F. Biological and analytical
characterization of two extracts from Valeriana officinalis. J. Ethnopharmacol. 2007; 112(2): 361-367.
18 Wheatley D. Medicinal plants for insomnia: a review of their pharmacology, efficacy and
tolerability. J. Psychopharmacol. 2005; 19(4): 414-421.
19 Lindahl O, Lindwall L. Double blind study of a valerian preparation. Pharmacol. Biochem.
Behav. 1989; 32: 1065-1066.
20 Khom S, Baburin I, Timin E, Hohaus A, Trauner G, Kopp B, Hering S. Valerenic acid
potentiates and inhibits GABA(A) receptors: Molecular mechanism and subunit specificity.
Neuropharmacology. 2007; [Epub ahead of print].
21 Sichardt K, Vissiennon Z, Koetter U, Brattström A, Nieber K. Modulation of postsynaptic
potentials in rat cortical neurons by valerian extracts macerated with different alcohols: involvement of
adenosine A(1)- and GABA(A)-receptors. Phytother. Res. 2007; [Epub ahead of print].
22 Lacher SK, Mayer R, Sichardt K, Nieber K, Müller CE. Interaction of valerian extracts of
different polarity with adenosine receptors: identification of isovaltrate as an inverse agonist at A1
receptors. Biochem Pharmacol. 2007; 73(2): 248-258.
23 Vo LT, Chan D, King RG. Investigation of the effects of peppermint oil and valerian on rat liver
and cultured human liver cells. Clin. Exp. Pharmacol. Physiol. 2003; 30(10): 799-804.
24 von der Hude W, Scheutwinkel-Reich M, Braun R. Bacterial mutagenicity of the tranquilizing
constituents of Valerianaceae roots. Mutat. Res. 1986; 169(1-2): 23-27.
25 [No authors listed]. Management of insomnia: a place for traditional herbal remedies. Prescrire
Int. 2005; 14(77): 104-107.
26 Gerhard U, Linnenbrink N, Georghiadou C, Hobi V. Vigilance-decreasing effects of 2 plant-
derived sedatives. Schweiz Rundisch Med Prax 1996; 85: 473-481.
27 Garges HP, Varia I, Doraiswamy PM. Cardiac complications and delirium associated with
valerian root withdrawal. JAMA 1998; 11: 1566-1567.
28 Khawaja IS, Marotta RF, Lippmann S. Herbal medicines as a factor in delirium. Psychiatr.
Serv. 1999; 50(7): 969-970.
29 Hellum BH, Hu Z, Nilsen OG. The induction of CYP1A2, CYP2D6 and CYP3A4 by six trade
herbal products in cultured primary human hepatocytes. Basic. Clin. Pharmacol. Toxicol. 2007;
100(1): 23-30.
30 Alkharfy KM, Frye RF. Effect of valerian, valerian/hops extracts, and valerenic acid on
glucuronidation In vitro. Xenobiotica. 2007; 37(2): 113-123.
31 Tufik S, Fujita K, Seabra Mde L, Lobo LL. Effects of a prolonged administration of
valepotriates in rats on the mothers and their offspring. J. Ethnopharmacol. 1994; 41(1-2): 39-44.
Source: http://www.arkopharma.it/mailing/2012-09/arkophytum-32/stress-e-sonno.pdf
NC Comprehensive School Health Training Center 8th Grade, Objective 8.03 Objective: Analyze the safe and effective use of methods of FDA-approved contraceptives to prevent unintended pregnancy. Materials: Appendix 1a, b– Stella's Story and teacher master Appendix 2a, b – Summary Table of Contraceptive Methods (background for teacher) 2007 FDA Birth Control Guide (see CD-ROM) PowerPoint – Contraceptives Contraceptives Kit with sample of methods of birth control Appendix 3a, b – template cut and taped to index cards. One set for each student, or pairs Different contraceptive examples (condoms, birth control pills, Nuvaring, Orthoevra) Appendix 4a, b– Public Service Announcement Template and scoring rubric Review: Assess students' recall of the O-M cycle and when conception is most likely to occur (G6, 2.07 Summarize the relationship between conception and the menstrual cycle). To begin our lesson, I would like to see what you recall about the ovulation-menstruation cycle and other changes that occur during puberty. I have a story that I will distribute and you will need to fill in the blanks using the word bank. Distribute "Stella's Story" (Appendix 1). Go over Teacher Key of "Stella's Story" (Appendix 2) and have students volunteer to fill in the blanks. Statement of Objectives: There are many reasons to delay parenthood and prevent unintended pregnancy. Today we will analyze the safe and effective use of methods of FDA-approved contraceptives to prevent unintended pregnancy as well as considerations for use. Focus: [Set up ahead of time the following bags of beans: Contraceptive implants (99 red beans; 1 white bean) Injectable contraceptives (99 red beans; 1 white bean) Oral contraceptives (95 red beans; 5 white beans) Contraceptive skin patch (95 red beans; 5 white beans) Vaginal contraceptive ring (95 red beans; 5 white beans) Male condom (85 red beans; 15 white beans) Female condom (80 red beans; 20 white beans) Contraceptive sponge (68 red beans; 32 white beans) Vaginal spermicides (70 red beans; 30 white beans) Withdrawal (73 red beans; 27 white bean)
Università degli Studi di Catania Scuola Superiore di Catania International PhD Investigation of Cancer Stem Cells (CSCs)-derived exosomes and their influence on the tumor microenvironment Coordinator of PhD Tutor Prof. Daniele Condorelli Prof. Ruggero De Maria a.a. 2008/2011 Agli uomini della mia vita Valerio e Riccardo







